核苷作为生命遗传物质的基础单元,已经成为现代药物研发的重要靶点,其在细胞内部有一套精密的“货币”系统,可以将核苷转化为磷酸化产物(核苷酸、核苷二/三磷酸),作为能量载体和信号分子。核苷类药物(如瑞德西韦)正是模仿了这些“生命货币”,进入细胞后,经过层层“加码”(磷酸化),最终变成“三磷酸”活性形式,精准打击病毒或癌细胞。
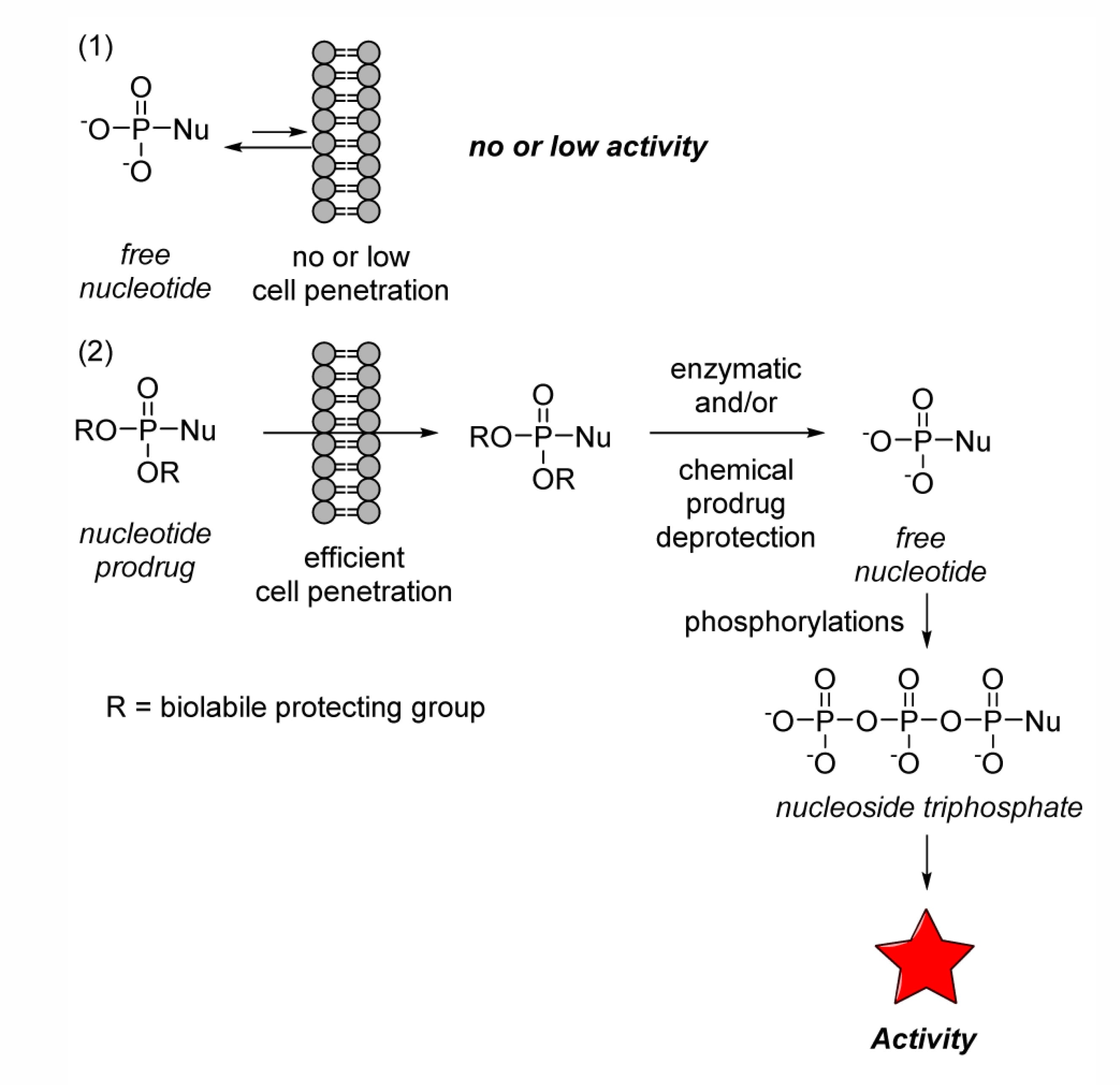
图1. 核苷单磷酸前药生物活性调控机制[1]
生物分析作为揭示核苷及其类似物体内命运的核心手段,面临了多种挑战,主要包括:
同分异构多:如同孪生兄弟,如ATP和dGTP分子量一致,结构差异细微,在液相上难以分离,分析时需要选择特定的色谱柱,并对流动相pH值进行精准调节。
代谢路径复杂:在激酶作用下,从原型药→单磷酸→二磷酸→三磷酸逐步转化,对原型药及其磷酸化形式进行多重分析时,需要对核苷代谢产物进行精准定量和分离。
极性强、不稳定:因磷酸基团具有强极性导致在色谱柱上难以保留,并且多磷酸形式易被磷酸酶酶解,分析过程中需要添加稳定剂。
基质干扰严重:生物样本中易受到内源性物质如内源性核苷酸(如cAMP、NAD+)的信号干扰,需采用同位素内标校正与替代基质定量。
面对上述挑战,液相色谱-串联质谱联用技术 (LC-MS/MS) 脱颖而出,成为分析核苷磷酸化通路的金标准。它如同精密的“分子显微镜”:
超强分离 (HPLC):将结构相似的“孪生兄弟”分开;
精准识别/定量 (MS/MS, MRM模式):高灵敏度、高选择性地追踪目标分子;
一箭双雕:既能定性确认身份,又能精确定量浓度;
高通量潜力:适应大规模样本分析;
LC-MS/MS技术不仅能精确定量原型药物(如瑞德西韦)及其关键磷酸化代谢物,也可以揭示药物-内源性核苷的相互作用,为阐释药效机制、耐药性的产生等提供数据支持。
本文将阐述核苷及其类似物作用机制(包括核苷-核苷酸-核苷磷酸及其类似物)、生物分析的最新进展,聚焦其“结构相似性-代谢复杂性-基质干扰性”三大难点,通过其在代谢疾病、免疫治疗等方面的案例系统评述建立核苷、核苷单磷酸、核苷二磷酸、核苷三磷酸LC-MS/MS分析平台的重要性,推动核苷磷酸相关疾病发现和精准医学发展。
核苷-核苷酸-核苷磷酸类化合物作用机制
核苷、核苷酸和核苷磷酸在生物体内通过相互转化与协同作用,共同参与了遗传信息传递、能量储存与转换以及细胞信号调控等核心生命过程。下文将介绍核苷、核苷酸、核苷磷酸的合成、代谢转化路径及其作用机制。
核苷
核苷是由含氮碱基和五碳糖通过糖苷键连接而成的化合物,分为核糖核苷和脱氧核糖核苷两类,是核糖核酸(包括DNA和RNA)的主要组成部分。核苷类似物是通过人工合成或化学修饰(碱基、糖环、糖苷键修饰)天然核苷结构获得的衍生物,此类化合物通常在体内被细胞内的激酶磷酸化成相应的核苷三磷酸类似物才能发挥主要作用。
核苷酸
核苷酸是由嘌呤或嘧啶碱基通过β-N-糖苷键与戊糖(核糖或脱氧核糖)1'位碳连接,再经5'-羟基磷酸酯化形成的化合物。其生物合成包含从头合成(小分子前体逐步组装碱基环)和补救合成(回收游离碱基或核苷)两条主要代谢途径。
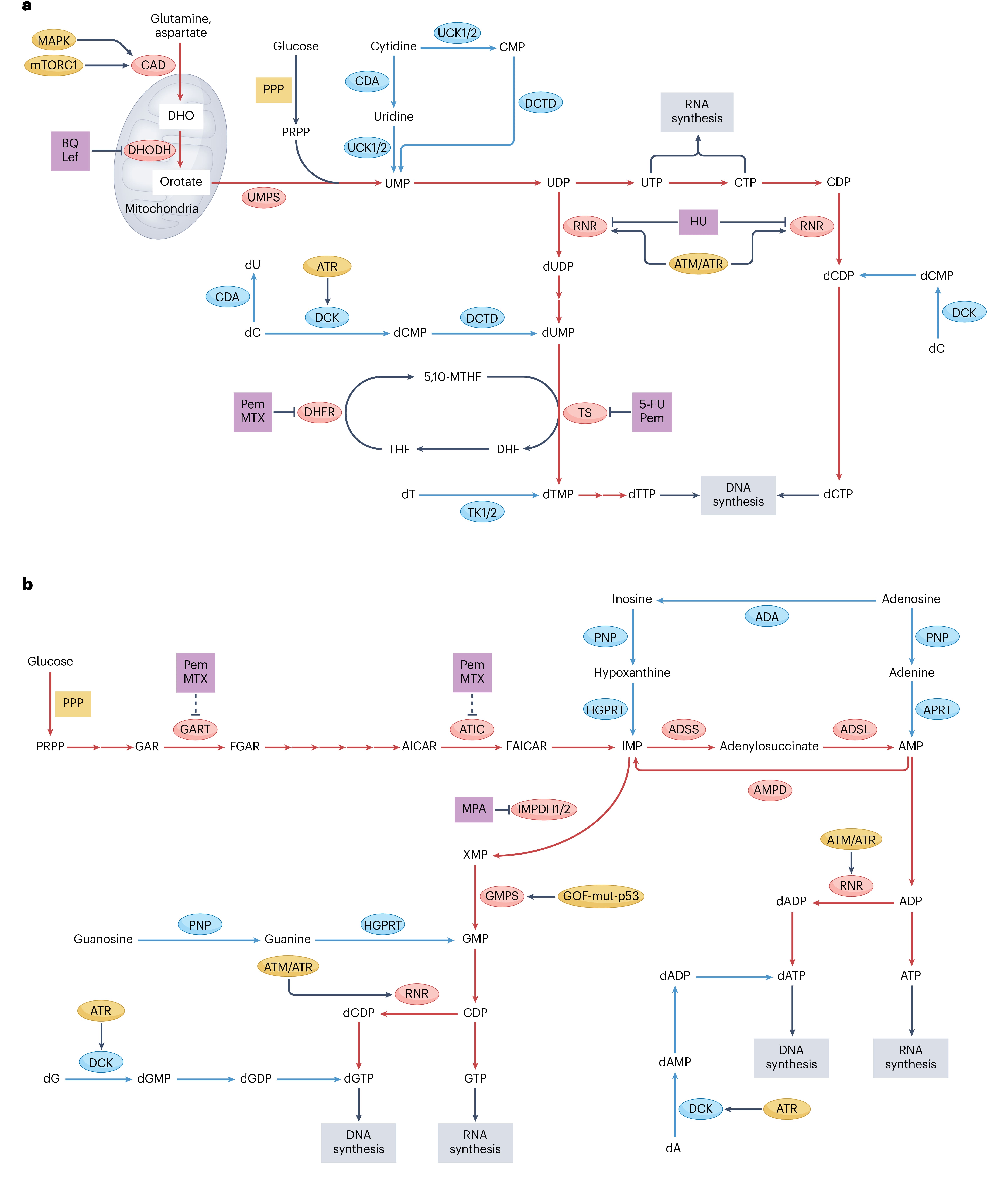
图2. 嘧啶和嘌呤核苷酸、相关抑制剂和致癌调节因子的生物合成途径[2]
核苷酸类似物保留了天然核苷酸的核心结构,至少有一个磷酸基团(P)与糖部分相连。其化学多样性基于如卤化、引入含氮基团(偶氮化)或掩蔽极性、提高脂溶性来增强口服吸收和靶向递送,在体内可控释放活性药物或者其他修饰过程,在抗病毒(如丙型肝炎病毒(HCV)、疱疹病毒 (HSV))和抗炎治疗中效果显著,其应用推动了前药设计、递送系统开发,为开发靶向核酸代谢的抗病毒/抗肿瘤药物奠定分子基础。
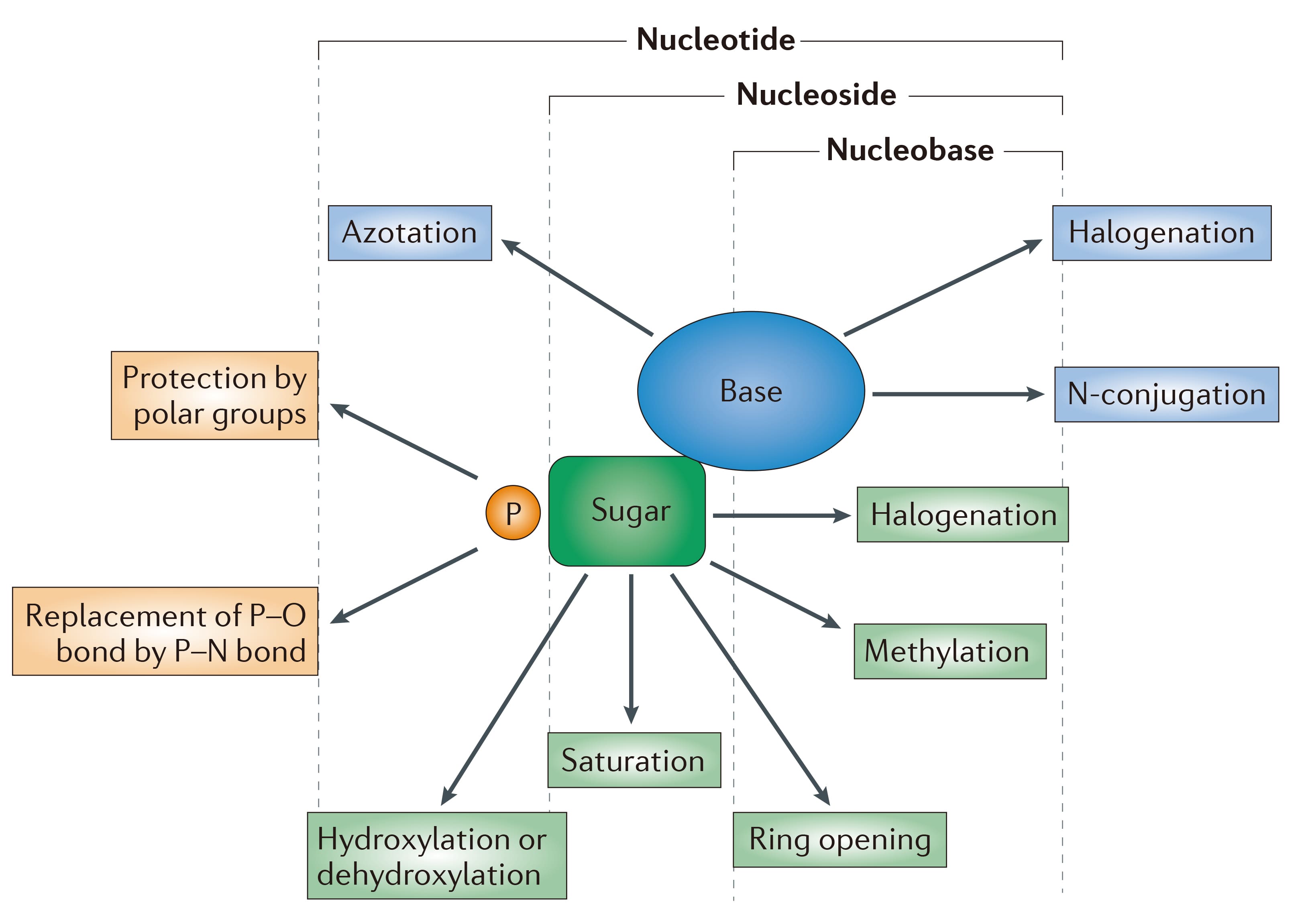
图3. 核苷酸类似物的一般结构和化学修饰[3]
核苷磷酸
核苷磷酸类化合物是天然核苷酸通过定向化学修饰,使其赋予独特的生物活性和药理特性,其生物合成依赖两条途径:在肝脏等组织中从简单的前体物质经过一系列的酶促反应合成;现有的核苷或碱基通过激酶的磷酸化补救途径生成。
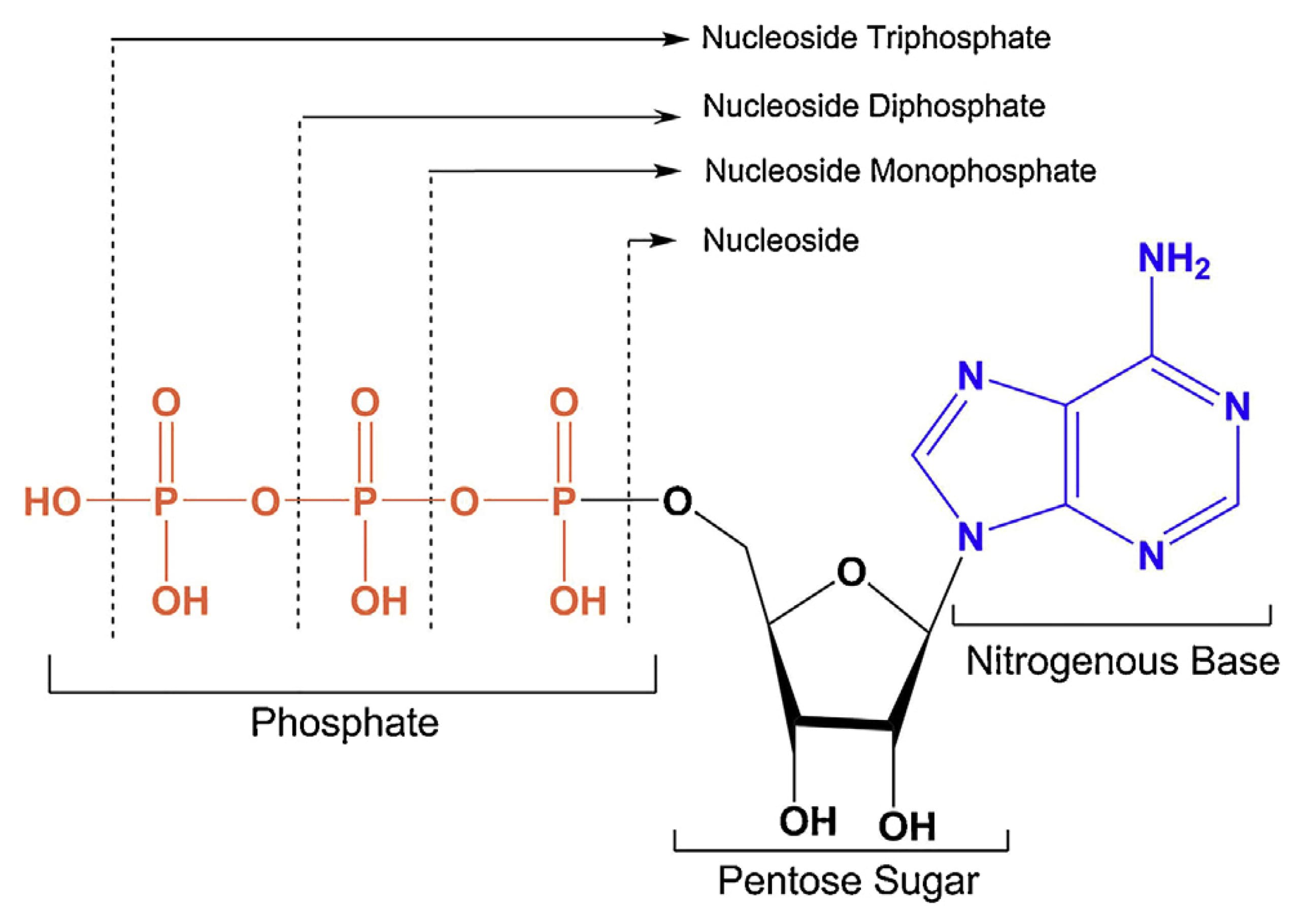
图4. 核苷三磷酸的代表性化学结构[4]
核苷、核苷酸及其类似物通过靶向核酸代谢酶,实现抗肿瘤、抗病毒作用,其作用机制的不断解析推动了药物设计的精准化,更揭示了其在疾病治疗中的潜在新靶点。
核苷及其类似物的治疗领域及趋势
核苷及核苷酸类药物在抗病毒、抗肿瘤及免疫调节等领域占有重要地位。从1953年起,靶向核苷酸已逐渐被设计为化疗药物用于治疗癌症,通过药物阻断核苷酸代谢来增强其免疫机能从而达到治疗效果。
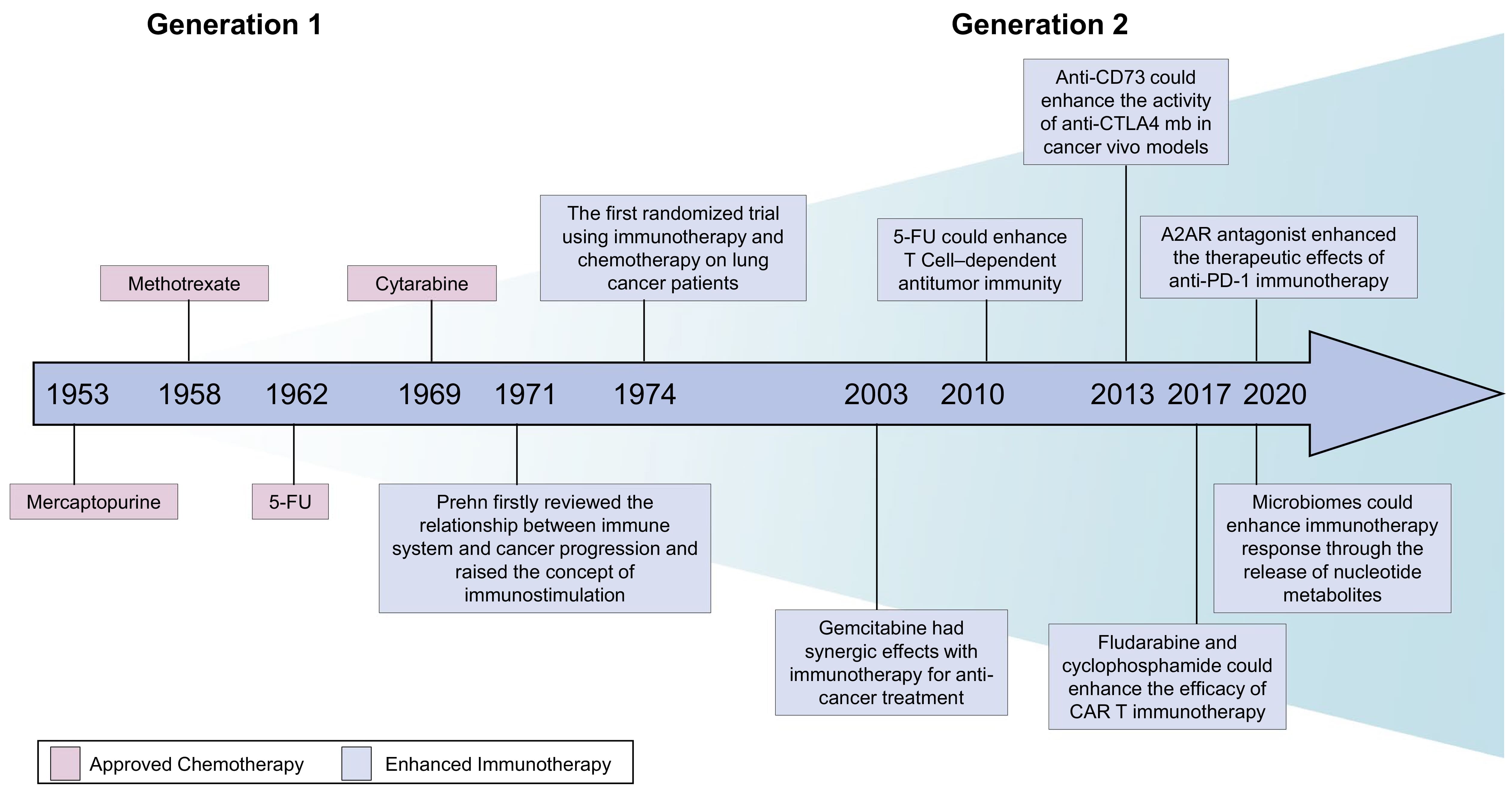
图5. 靶向核苷酸代谢在癌症治疗中的历史发展与突破[5]
近年来,随着病毒性肝炎、艾滋病及肿瘤等重大疾病发病率的攀升,核苷及核苷磷酸类药物市场需求持续扩大,在全球医药市场中占有较为重要的份额。
表1. 全球核苷及核苷磷酸类代表性上市药物
药物名称 | 适应症 | 研发公司 | 上市时间 |
艾米替诺福韦 | 慢性乙型肝炎 | 吉利德科学 | 2016 |
艾米替诺福韦(中国产) | 慢性乙型肝炎 | 豪森药业 | 2021 |
格卡瑞韦/哌仑他韦 | 泛基因型丙型肝炎 | 艾伯维 | 2018 |
可洛派韦 | 丙型肝炎 | 歌礼制药 | 2022 |
多替拉韦/拉米夫定 | HIV感染 | 葛兰素史克 | 2019 |
瑞德西韦 | COVID-19(住院患者) | 吉利德科学 | 2020 |
核苷及其类似物药物倾向于参与DNA或RNA复制过程的酶相互作用,从而达到抑制病毒或癌细胞的生命周期的作用。核苷类药物在病毒复制过程中,可以有效阻断病毒 RNA 链延伸,提前终止病毒复制,从而实现抗病毒的作用。瑞德西韦作为腺嘌呤核苷类似物前药,其1'-氰基修饰的磷酰胺结构经细胞质羧酸酯酶水解后,依次转化为中间体GS-441524单磷酸盐及终活性三磷酸代谢物GS-443902。该三磷酸代谢物通过模拟ATP竞争性抑制病毒RdRp(IC50 = 1.1 μM),导致病毒RNA链合成终止,从而发挥抗SARS-CoV-2作用[6]。
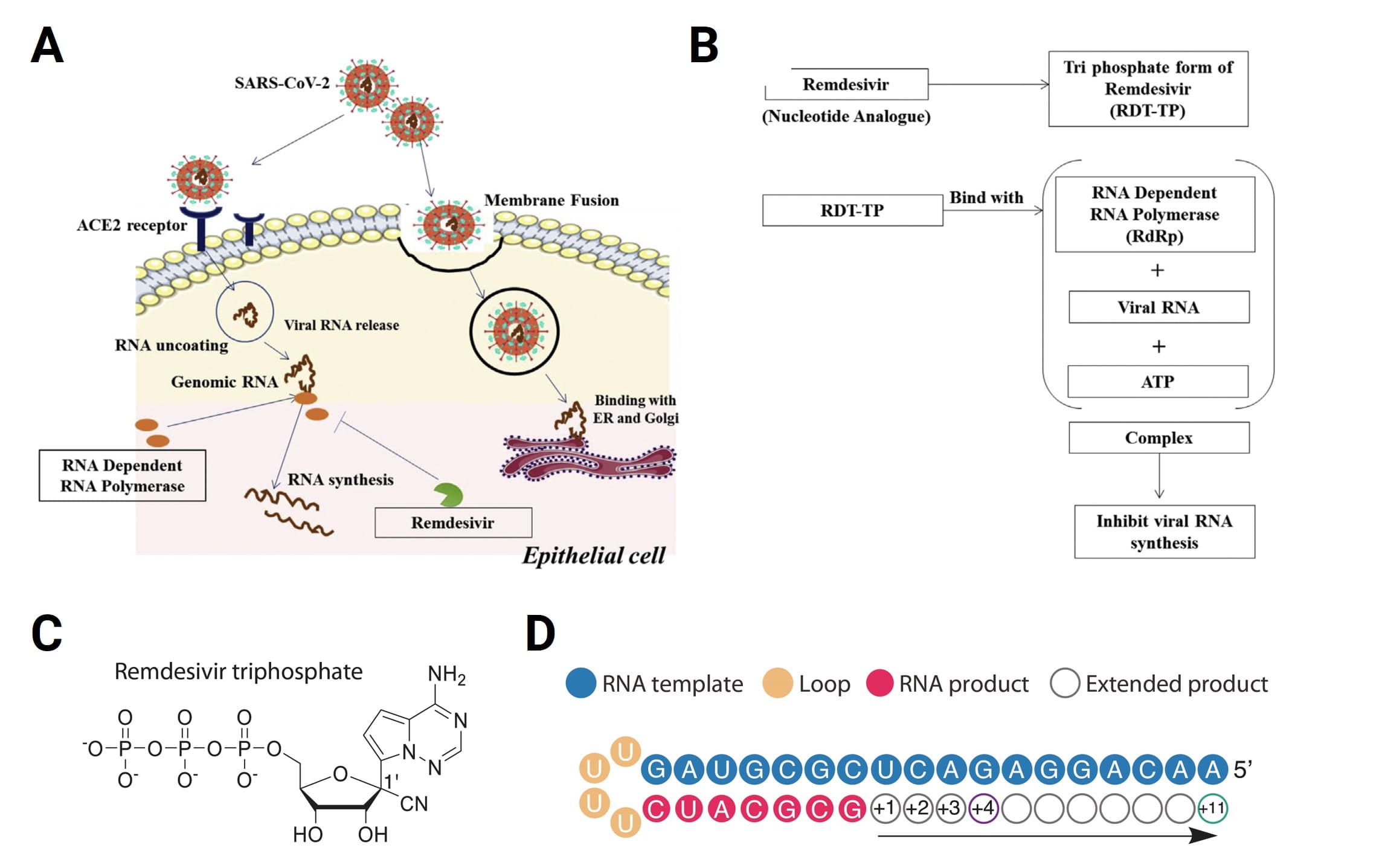
图6. 瑞德西韦抑制 SARSCoV-2病毒复制分子机制及阻碍 RNA 延伸[7,8]
核苷磷酸在其他方面也具有多维度核心功能:抗癌方面通过靶向抑制核苷酸代谢关键酶(如TSase),阻断癌细胞增殖与转移依赖的代谢重编程路径;代谢调控领域,其5′-单/二/三磷酸前药设计显著提升药物活化效率,同时通过端粒酶介导的核苷磷酸代谢参与抗衰机制;在基础研究层面,对激酶/磷酸酶等代谢酶的结构解析为靶向药物设计提供了精准的分子基础,由此形成的机制探索至临床转化的完整研究链条,推动了药物研发的突破。与此同时,作为遗传信息载体,mRNA疫苗通过碱基修饰(如修饰核苷)实现了类似于表观遗传调控的精准化,该技术因在疾病治疗中的革新性应用获得2023年诺贝尔奖。
鉴于核苷及其磷酸化产物通过干预核苷代谢网络展现出来的多靶点治疗潜力,建立精准的定量分析方法成为解析其组织分布动态、优化药代动力学-药效学的关键技术支柱。
核苷及其磷酸类化合物分析平台
核苷及其磷酸类化合物的分析难度大,缺乏系统化的分析平台和分析策略。基于化合物特性与检测难点,从样品前处理、色谱分离优化等维度对核苷原药、核苷代谢通路中转化的核苷单磷酸/二磷酸/三磷酸提出针对性的分析方法。
核苷原型药
以核苷类似物前药瑞德西韦为例,为克服瑞德西韦的化学不稳定性,药明康德DMPK研究开发了稳定剂配方,有效解决了其代谢物降解问题,并基于液相色谱-串联质谱(LC-MS/MS)技术实现了对其及主要代谢物的分离和定量分析。
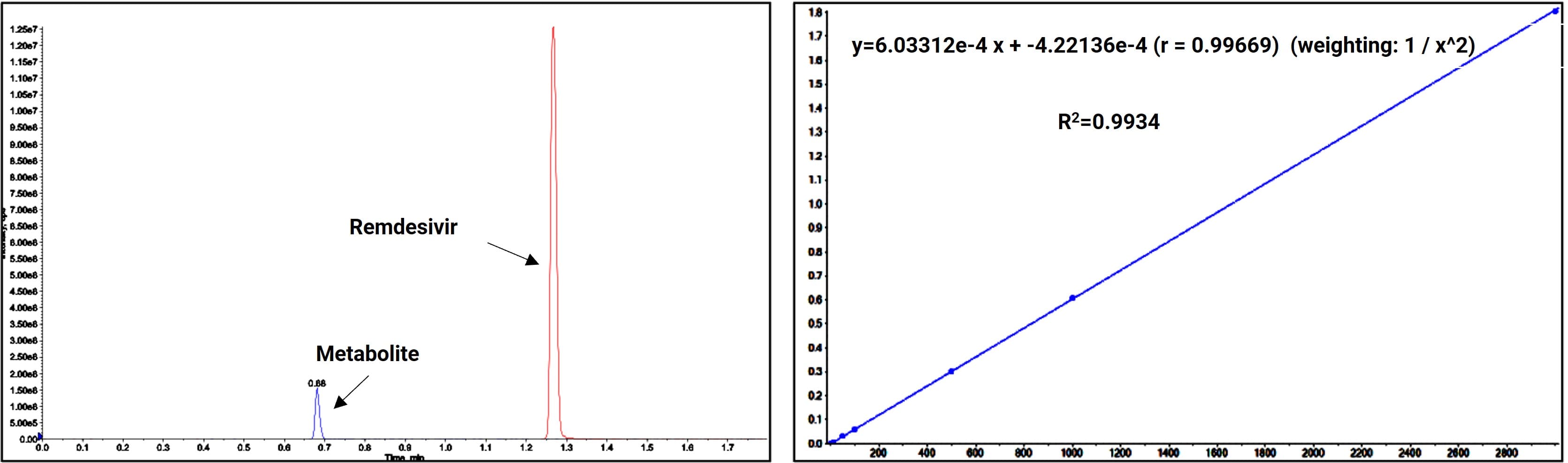
图7. 瑞德西韦代谢物的分离分析及线性拟合图
上述建立的方法成功实现了瑞德西韦原型药物的高灵敏度、高选择性定量分析,在两分钟内可以对瑞德西韦及其代谢物同时进行分析,检测限达到2 ng/mL以下。然而瑞德西韦的抗病毒活性主要依赖于其在细胞内逐步磷酸化的三磷酸代谢产物。在这一关键的活化路径中,核苷单磷酸、核苷二磷酸是重要的中间代谢物。对于这两类核苷磷酸的分析使我们深入了解药物的药代动力学行为及潜在的药效-毒性之间的关联。下文将重点介绍核苷单磷酸、核苷二磷酸及核苷三磷酸的分析方法策略。
核苷单磷酸
核苷单磷酸化合物属于酸性化合物,具有良好的水溶性,因为磷酸基团容易与水分子形成氢键,在色谱柱上难以保留。药明康德DMPK使用LC-MS/MS建立核苷单磷酸分析方法,主要流程在于:
优化前处理方法、液相条件可以让核苷单磷酸有效地保留;
通过筛选稳定剂解决核苷单磷酸与核苷化合物的稳定性问题;
改变流动相的pH值、梯度及选择合适的色谱柱减少峰形拖尾和残留等情况;
优化条件使用较为常见的流动相(水/乙腈体系)进行分析,简化了方法流程。
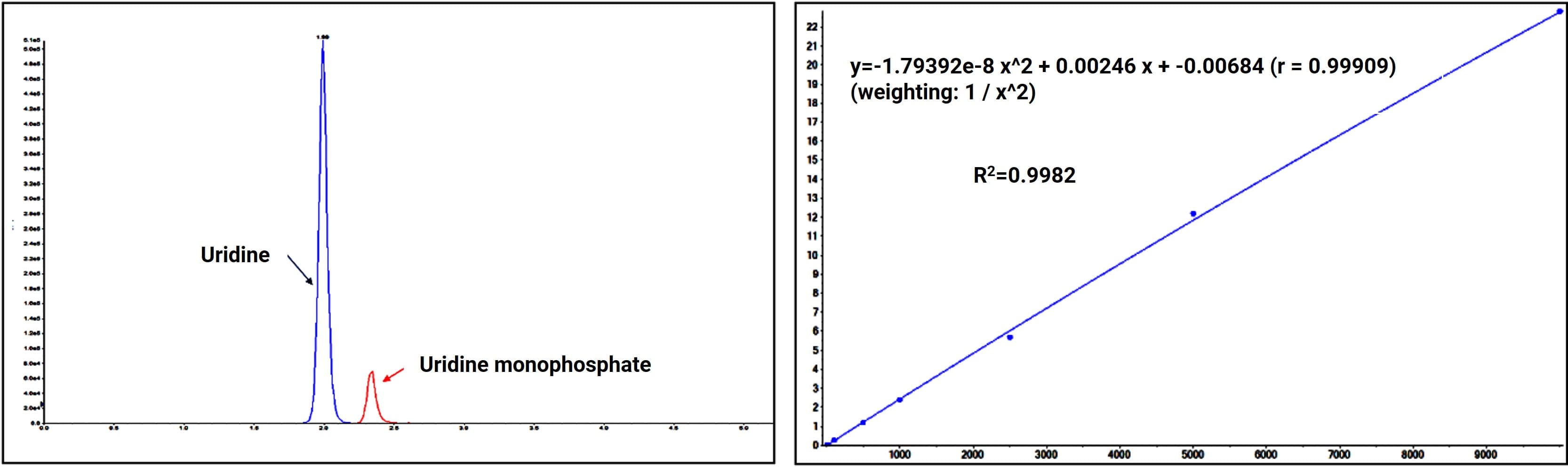
图8. 尿苷与尿苷单磷酸的分离分析及线性拟合图
药明康德DMPK通过不断探索和优化,总结了一套完整的分析流程(如尿苷与尿苷单磷酸),能够快速解决核苷单磷酸化合物的峰形、保留、稳定性等问题,高质高效完成项目分析。
核苷二磷酸
核苷二磷酸结构中有两个磷酸基团,酸性较强,极性增加,通过两个磷酸基团之间的高能磷酸键,储存和释放能量,参与磷脂和糖原的合成,比如UDP-葡萄糖通过葡萄糖-1-磷酸与UTP(尿苷三磷酸)反应生成,并通过糖原合成酶参与糖原的合成反应,在肝脏和肌肉内发挥作用。
药明康德DMPK突破传统双通路离子对流动相体系,开发出了单通路离子对LC-MS/MS方法,显著提升核苷二磷酸类化合物分析方法开发效率。通过持续迭代,相关试剂用量大幅度下降,色谱柱耐用程度大幅度提升,在实现绿色节能同时,单样品分析成本显著下降。
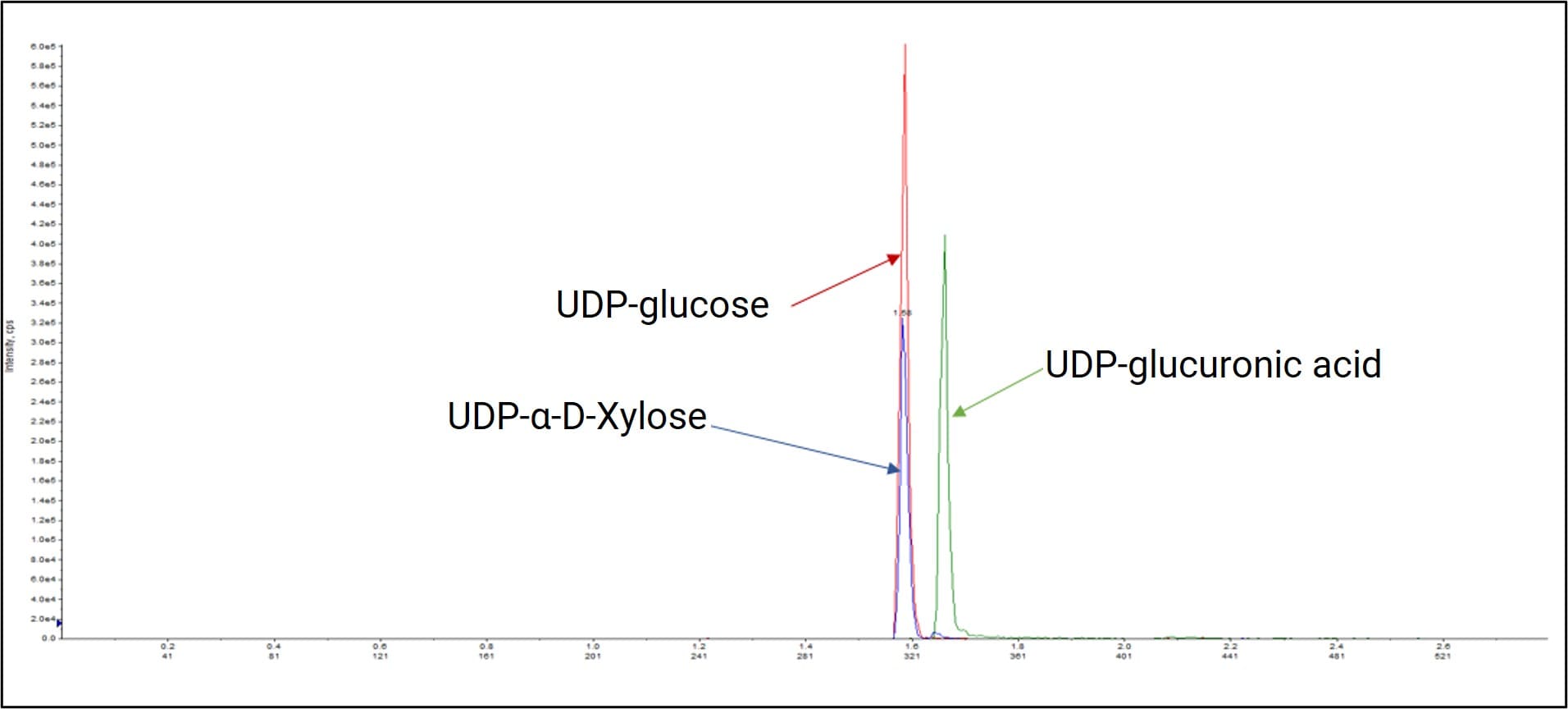
图9. UDP-葡萄糖类在LC-MS/MS中的分离分析
表2. 优化前后的方法结果对比
| Basic LC condition | Acidic LC condition |
Amount of ion-pairing reagent | 32.3 g/10,000 injections | 7.32 g/10,000 injections (-77.3%) |
Column lifetime | ~300 injections | ~1000 injections |
核苷三磷酸
核苷三磷酸化合物中三个磷酸基团之间的高能磷酸键(尤其是β和γ磷酸之间的键),在水解时释放大量能量,参与DNA与RNA的合成,在体内调控各种生理作用。
利巴韦林(RBV)用于治疗丙型肝炎病毒,通过其活性磷酸化代谢物利巴韦林5'-三磷酸(RTP)感染发挥抗病毒作用。药明康德DMPK针对生物分析中内源性尿苷三磷酸与目标物RTP的同分子量干扰难题,开发出高选择性LC-MS/MS方法,成功实现两者基线分离,并在红细胞及肝脏组织基质中完成验证,消除内源干扰影响。
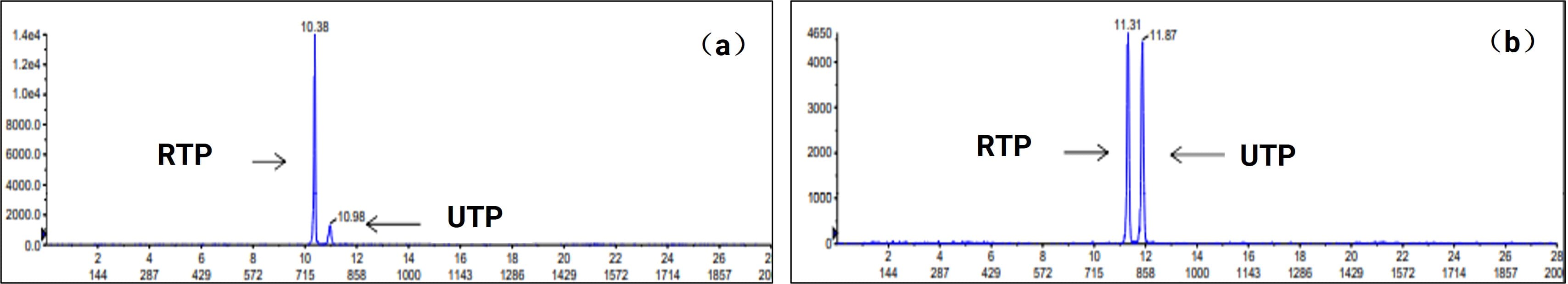
图10. RTP与UTP在LC-MS/MS中的分离分析基质类型为(a)红细胞 (b)肝脏
针对核苷三磷酸(NTP)在肝脏等靶器官内会动态转化而导致的分离难题,药明康德DMPK开发的LC-MS/MS方法实现关键突破:
高通量多组分同步检测:单针进样完成6种NTP/dNTP定量(12分钟/样本);
同分异构体精准分离:优化色谱柱选择性实现dGTP/ATP这对同分异构体的基线分离;
超高灵敏度检测:提升质谱离子化效率,基质中LLOQ达10 ng/mL ;
消除磷酸基团拖尾问题:流动相pH梯度优化获得对称峰形;
内源性干扰破解:替代基质快速筛选策略;
全流程稳定性保障:通过筛选含氟化钠等稳定剂,保证在匀浆-样品前处理-分析过程中处于稳定状态。
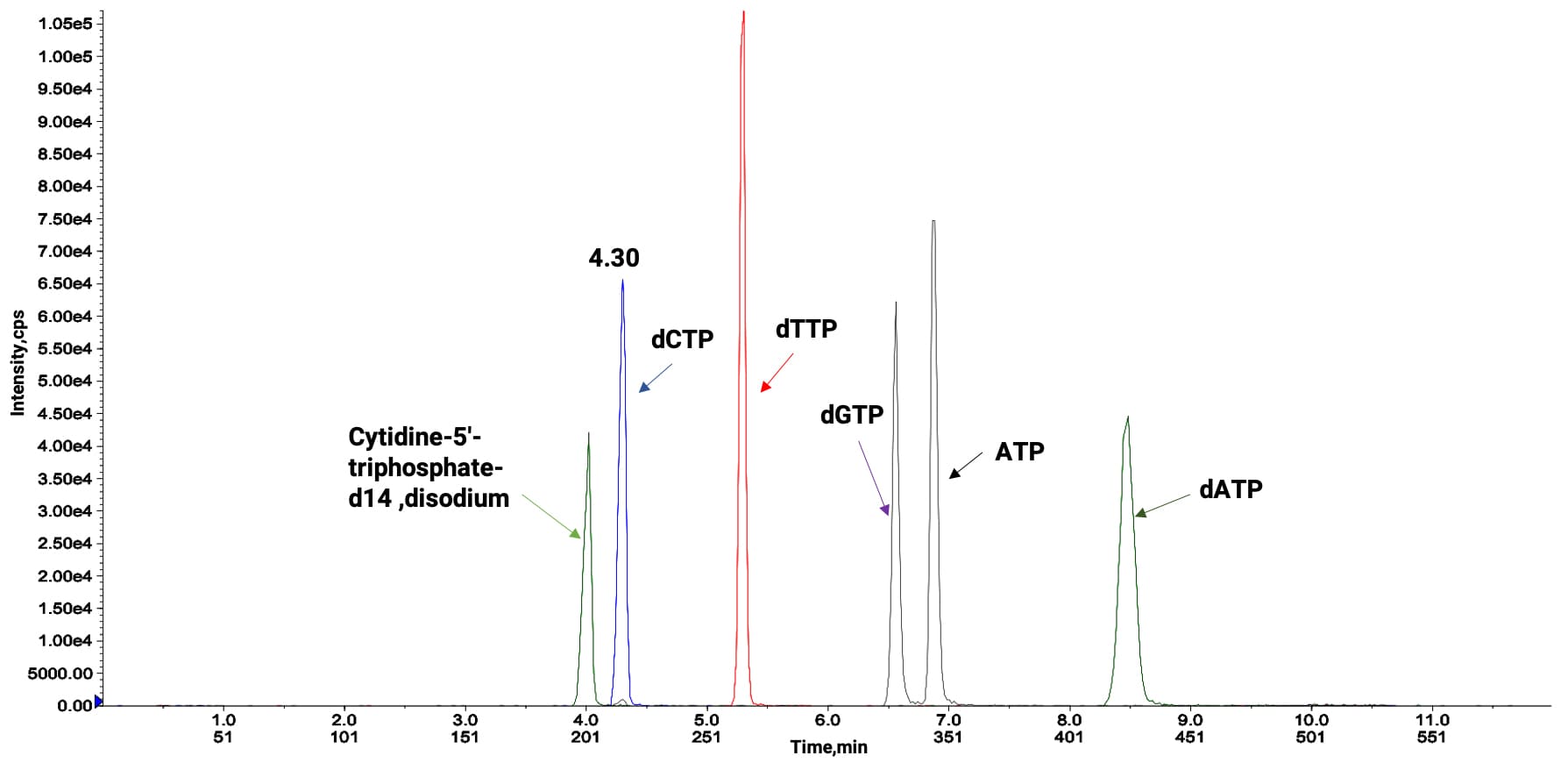
图11. 几种标志性NTP在LC-MS/MS中的分离分析
结语
药明康德DMPK依托LC-MS/MS核苷磷酸分析平台,不仅能精准定量,更能深入解析:
追踪活化之路:实时监测前药(如瑞德西韦)在肝细胞内如何逐步磷酸化为活性三磷酸形式。
洞察全局影响:结合代谢组学,分析药物干预下内源性核苷酸代谢网络(能量代谢、核酸合成等)的变化,揭示潜在作用机制或脱靶效应。
手性分离:利用手性色谱柱精准分离核苷类对映异构体。
多维数据支撑:为药效评价、药代动力学(PK)、药效动力学(PD)及申报注册提供全面、可靠的数据基石。
药明康德DMPK已构建覆盖核苷→单磷酸→二磷酸→三磷酸全链条的成熟LC-MS/MS分析体系,成功解决稳定性、保留、分离、干扰、定量等核心挑战。我们致力于为全球合作伙伴提供高质量、高效的生物分析数据,加速核苷类药物从靶点发现到临床转化的进程,共同推动精准医疗新时代。

图12. 药明康德DMPK质谱分析平台
作者:张烁,张显春,龚武云,李陟昱,邢丽丽
编辑:富罗娜·克里木,钱卉娟
设计:倪德伟,张莹莹
药明康德DMPK依托中国(上海、苏州、南京和南通)和美国(新泽西)的研发中心,提供从早期筛选、临床前开发、到临床研究阶段的综合型药代动力学服务,助力您快速推进药物研发流程。拥有上千人的研发团队,服务超1600家全球客户,具有超过十五年的新药申报经验,已成功支持超过1700个新药临床研究申请(IND)。
点击此处与我们的专家进行联系
参考
[1] Pradere U, Garnier-Amblard EC, Coats SJ, Amblard F, Schinazi RF. Synthesis of nucleoside phosphate and phosphonate prodrugs. Chem Rev. 2014 Sep 24;114(18):9154-218. doi: 10.1021/cr5002035.
[2] Mullen NJ, Singh PK. Nucleotide metabolism: a pan-cancer metabolic dependency. Nat Rev Cancer. 2023 May;23(5):275-294. doi: 10.1038/s41568-023-00557-7.
[3] Jordheim LP, Durantel D, Zoulim F, Dumontet C. Advances in the development of nucleoside and nucleotide analogues for cancer and viral diseases. Nat Rev Drug Discov. 2013 Jun;12(6):447-64. doi: 10.1038/nrd4010.
[4] Gautam N, Alamoudi JA, Kumar S, Alnouti Y. Direct and indirect quantification of phosphate metabolites of nucleoside analogs in biological samples. J Pharm Biomed Anal. 2020 Jan 30;178:112902. doi: 10.1016/j.jpba.2019.112902.
[5] Wu HL, Gong Y, Ji P, Xie YF, Jiang YZ, Liu GY. Targeting nucleotide metabolism: a promising approach to enhance cancer immunotherapy. J Hematol Oncol. 2022 Apr 27;15(1):45. doi: 10.1186/s13045-022-01263-x.
[6] Cox RM, Wolf JD, Lieber CM, Sourimant J, Lin MJ, Babusis D, DuPont V, Chan J, Barrett KT, Lye D, Kalla R, Chun K, Mackman RL, Ye C, Cihlar T, Martinez-Sobrido L, Greninger AL, Bilello JP, Plemper RK. Oral prodrug of remdesivir parent GS-441524 is efficacious against SARS-CoV-2 in ferrets. Nat Commun. 2021 Nov 5;12(1):6415. doi: 10.1038/s41467-021-26760-4.
[7] Saha A, Sharma AR, Bhattacharya M, Sharma G, Lee SS, Chakraborty C. Probable Molecular Mechanism of Remdesivir for the Treatment of COVID-19: Need to Know More. Arch Med Res. 2020 Aug;51(6):585-586. doi: 10.1016/j.arcmed.2020.05.001. Epub 2020 May 12. PMID: 32439198; PMCID: PMC7214327.
[8] Kokic G, Hillen HS, Tegunov D, Dienemann C, Seitz F, Schmitzova J, Farnung L, Siewert A, Höbartner C, Cramer P. Mechanism of SARS-CoV-2 polymerase stalling by remdesivir. Nat Commun. 2021 Jan 12;12(1):279. doi: 10.1038/s41467-020-20542-0.
加入订阅
获取药物代谢与药代动力学最新专业内容和信息