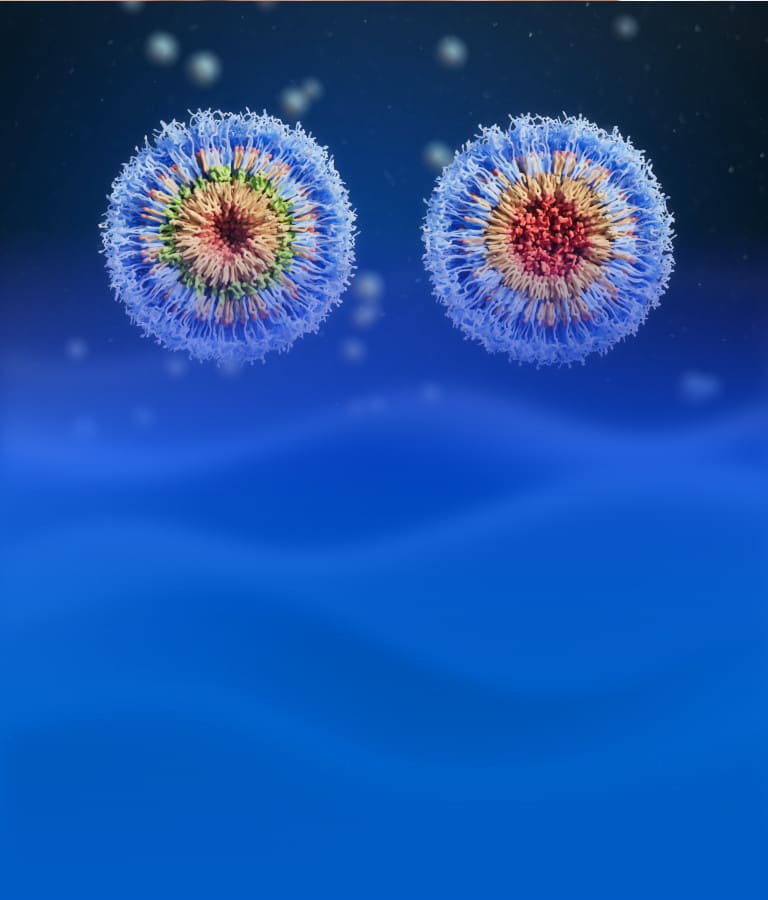
脂质体主要是由磷脂和胆固醇组成的纳米大小、具有脂质双分子层的封闭囊泡。亲水性化合物被包裹在脂质体亲水核区,疏水性化合物被包裹在磷脂双分子层的疏水区,结构见图1[1]。
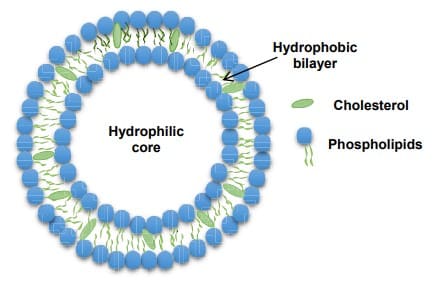
图1. 脂质体结构
根据研究目的不同,通过对脂质体的组分(不同的磷脂和胆固醇含量)、表面电荷(由组成磷脂的电荷产生)等方面进行修饰,可以制备用于延长循环时间的长循环脂质体(例如PEG修饰),用于基因药物载体的阳离子脂质体(修饰成带正电),在特定部位响应性释药的微环境敏感脂质体(体内pH、酶等微环境变化,或光、热效应等物理条件控制)以及提高靶向性(例如连接抗体)的免疫型脂质体等[1,2]。基于如上特征,H. Nsairatet al.[1]对已上市的脂质体药物的临床应用进行了总结,具体见表1。
表1. 小分子脂质体药物的临床应用
Usage | Trade name | Active ingredient(s) | Liposome platform (Molar Ratio) | Manufacture | Year Approved |
抗肿瘤 | Doxil® | Doxorubicin | HSPC:Cholesterol:PEG 2000-DSPE (56:38:5) | Sequus Pharmaceuticals | 1995 |
DaunoXome® | Daunorubicin | DSPC:Cholesterol (2:1) | NeXstar Pharmaceuticals | 1996 | |
Depocyt® | Cytarabine | DepoFoam™ | SkyPharma Inc. | 1999 | |
Myocet® | Doxorubicin | Cholesterol:EPC (45:55) | Elan Pharmaceuticals | 2000 | |
Mepact® | Mefamurtide | DOPS:POPC (3:7) Multilamellar liposome | Takeda Pharmaceutical Limited | 2004 | |
Lipodox® | Doxorubicin | DSPC:Cholesterol:PEG 2000-DSPE (56:39:5) | Sun Pharma | 2012 | |
Marqibo® | Vincristine | SM:Cholesterol (60:40) | Talon Therapeutics | 2012 | |
OnivydeTM | Irinotecan | DSPC:Cholesterol:MPEG-2000-DSPE (3:2:0.015) | Merrimack Pharmaceuticals | 2015 | |
Lipusu® | Paclitaxel | NA | Luye Pharma Group | 2006 | |
Vyxeos® | Cytarabine:Dau-norubicin 5:1 | DSPC:DSPG:Cholesterol (7:2:1) | Jazz Pharmaceuticals | 2017 | |
抗真菌 | Ambisome® | Amphotericin B | HSPC:Cholesterol:DSPG (2:1:0.8) | Astellas Pharma | 1997 |
Fungisome® | Amphotericin B | PC:Cholesterol (7:3) | Lifecare Innovations | 2003 | |
光能疗法 | Visudyne® | Verteporphin | Verteporphin:DMPC&EPG (1:8) | Novartis AG | 2000 |
镇痛 | DepoDurTM | Morphine sulfate | DepoFoam™ | SkyPharma | 2004 |
Exparel® | Bupivacaine | DepoFoam™ | Pacira pharmaceuticals | 2011 |
脂质体作为载体类纳米药物,与普通药物相比,其特殊的纳米粒径、磷脂双分子层结构以及特有的表面修饰等,使该药物的理化性质和生物学行为发生变化。普通药物的体内吸收特征主要通过测定体循环中的游离型药物浓度来体现,而脂质体药物与普通药物的区别在于其功能单位“载药粒子”的存在,该类药物在进入体内后,会以游离型(从脂质体中释放出来的药物,在体内主要以游离和血浆蛋白结合两种形态存在)与负载型(存在于脂质体中未被释放的药物)药物的形式存在,见图2。因此,在进行药代动力学研究时需要分别测定血液中游离型药物和负载型药物的浓度[3]。
由于脂质体制剂这些特定的临床优势,以及特有的药代动力学特征,近些年来该制剂的体内药物研究越来越火热。随着监管机构对于纳米粒技术的非临床药代动力学的研究及要求越来越成熟,建立一个重现性好、耐用性强、能够准确测定生物样本中游离型和负载型药物的方法很有必要。
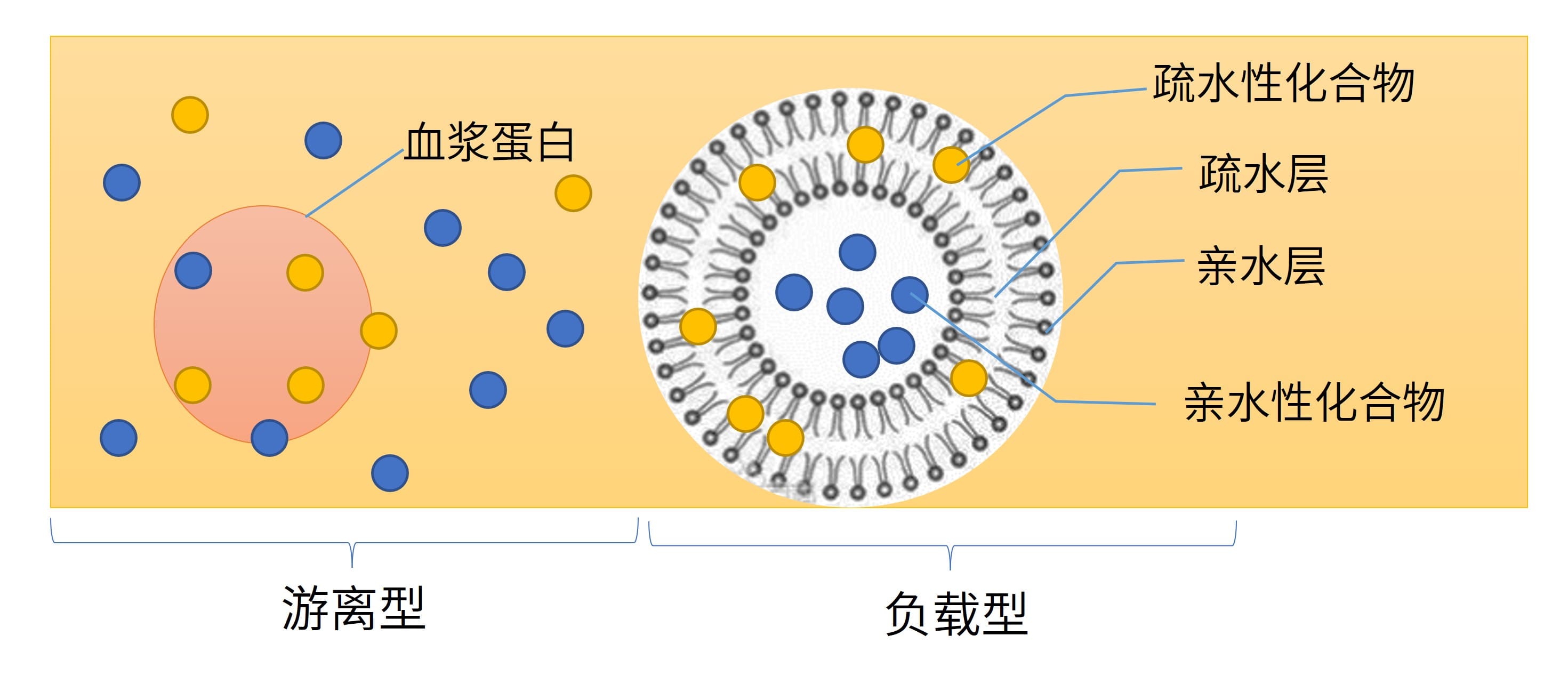
图2. 脂质体药物在体内的存在形态
在生物样本检测方法建立过程中,与普通药物相比,游离型和负载型药物的分离以及如何保证含有脂质体的生物样本在储存、前处理过程中的稳定是方法开发过程中所面临的挑战。由此而涉及到的校正标样及质控样本的制备、基质效应、选择性、回收率、稳定性甚至离心转速等方法开发方面,都有着与普通药物不同的考量。本文将基于对法规的理解和已有的项目经验,对该类型药物生物样本检测过程中需要关注的要点进行介绍。
脂质体药物在生物样本中检测方法建立的考量因素
与普通药相比,该类药物在体内的存在形态复杂,因此在生物分析方法建立过程中,如下内容需要额外关注。
分离方法的选择
对于体内游离型/负载型药物的测定无论是直接法(测定游离型和载药型)还是间接法(测定总药和游离型),为保证测定的准确性,两种方法在样品处理和分离过程中,均需确保载药粒子、游离型药物等不同形态成分的状态不发生变化。分离生物样本中游离型/负载型药物的常用方法包括平衡透析、超速离心、超滤、固相萃取(SPE)等[3]。根据实验目的不同,可以选用合适的方法进行分离检测。我们对这几类方法进行简单介绍,详见表2。
表2. 分离方法的选择
分离方法 | 原理 | 分离状态 | 适用范围 |
平衡透析 | 在半透膜两侧、仅允许小分子透过而大分子不能透过。 | F-F透膜,F-P保留在L部分 | 不吸附于半透膜的待测物,且脂质体制剂在该缓冲液中稳定 |
超速离心 | 不同强度的离心力使具有不同质量的物质分级分离。 | F-F,F-P以及L均可发生分离 | 亲水性化合物,成分单一的脂质体制剂 |
超滤 | 小分子药物在离心力的作用下可通过超滤膜,而大分子则被截留。 | F-F透膜,F-P保留在L部分 | 亲水性化合物,较低的蛋白结合率 |
固相萃取 | 填料与化合物之间的静电或疏水相互作用力将游离型化合物保留在填料上,负载型药物直接通过不被保留。 | F和L完全分离 | 能够被SPE的固定相吸附的待测物 |
F:游离型
F-F:游离型,指非血浆蛋白结合的游离部分
F-P:游离型,与血浆蛋白结合的游离部分
L:负载型,特指脂质体
平衡透析法耗时较长,对于蛋白结合率高的药物,游离型中游离态的浓度较低,对检测的灵敏度要求较高;超速离心法其较强的离心力作用可能会导致微粒聚集,破坏脂质体双分子层结构,导致药物发生泄漏;固相萃取法要求待测物能够被固相填料吸附,且脂质体双分子层表面组分不与固相填料发生作用,能够顺利通过填料颗粒间的空隙流出;超滤法适用于蛋白结合率低的亲水性化合物,与固相萃取法起到互补的作用。如上方法,可以根据实际的工作需求进行选择,固相萃取法和超滤法是脂质体类药物生物样本检测过程常用的分离方法(操作步骤可参考图3和图4)。
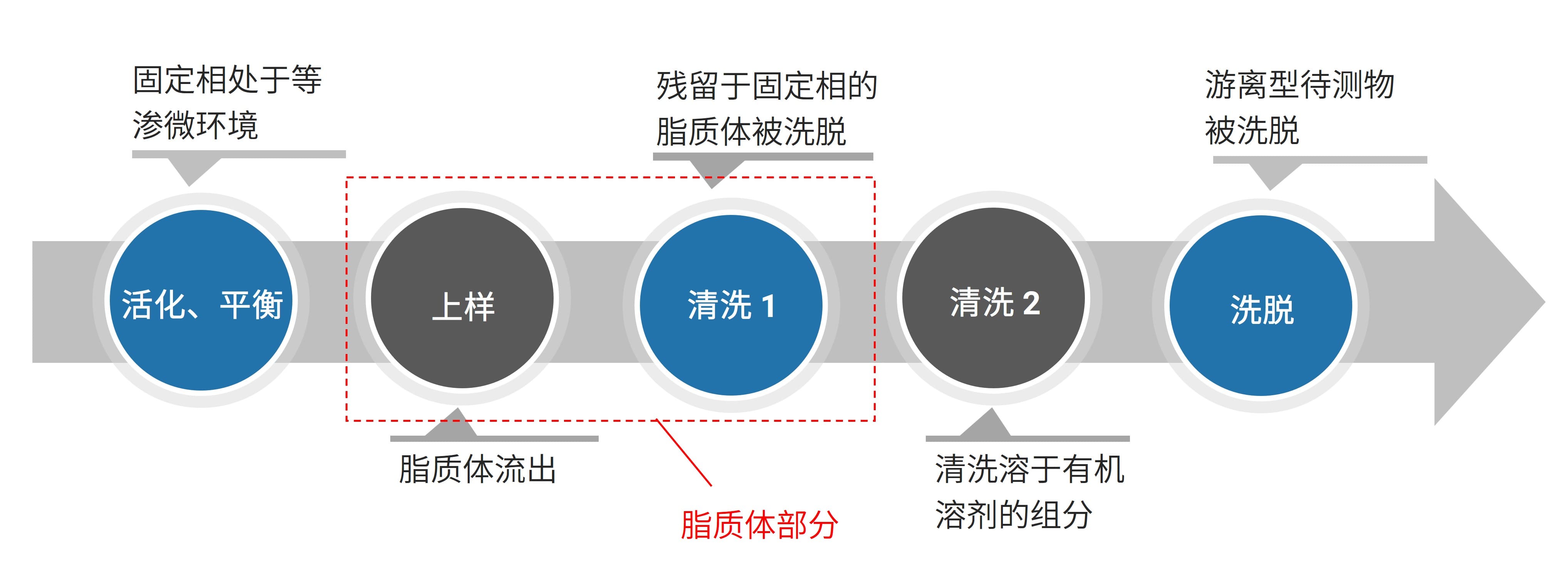
图3. SPE的一般流程
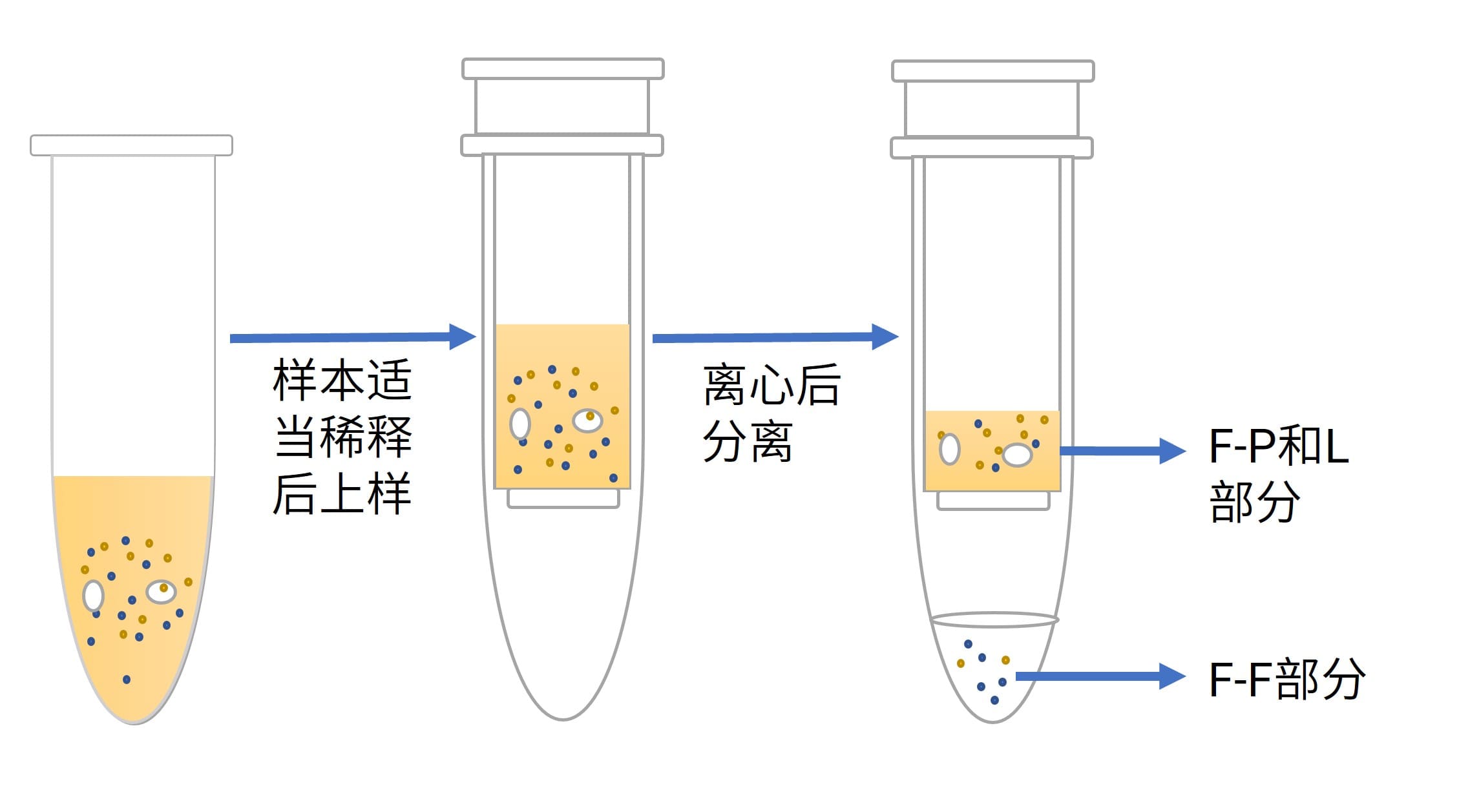
图4. 超滤法的一般流程
校正标样的制备
《纳米药物非临床药代动力学研究技术指导原则》中指出,建立载体类纳米药物体内分析方法学时,建议校正标样及质控样本模拟给药后载药粒子、游离型药物、负载型药物、载体材料的体内实际状态进行制备。
对于总药测定:根据预试验结果初步了解体内样品不同时间点游离型和负载型药物的浓度差异,模拟给药后游离型和负载型的体内状态,按照一定比例制备校正标样。
对于游离型测定:考虑到游离型药物体内浓度较低(浓度一般<20%总药),以及可能受脂质体包封率的影响,一般不建议使用脂质体和游离型药物混合的方式制备校正标样。采用游离型药物制备校正标样时,由于共存脂质体表面的磷脂及电荷等存在,可能与药物发生非特异性吸附,需要考虑到共存的脂质体可能导致游离型药物被洗脱。
对于负载型测定:要求相同批次不同瓶脂质体制剂在溶液状态下的包封率一致,且稳定性良好。可以直接使用脂质体配制到基质中制备校正标样,由于需要模拟体内状态,其浓度一般为游离型药物的数倍甚至数十倍,需要考察脂质体在前处理过程中的稳定性,以及万一发生渗漏后对游离型药物的浓度贡献影响。
验证考察项额外关注点
参考2022年8月中国药品监督管理局药品审评中心发布的《M10:生物分析方法验证与样品分析》指导原则实施建议中所涉及到的验证内容,结合实际工作需求,我们对于需要额外关注的地方进行了总结,具体见表3。
表3.方法开发中额外需要关注的验证内容
验证考察项 | 常规小分子 | 脂质体药物 | ||
总药 | 游离型 | 负载型 | ||
校正标样和质控样本的制备 | 血浆+游离型 | 血浆+游离型+负载型 | 血浆+游离型 | 血浆+负载型 |
选择性 | 6个来源的空白基质 | 需额外关注含有高浓度空白脂质体制剂血浆的选择型 | ||
基质效应 | 6个来源的空白基质、溶血基质效应(如需要) | 无额外增加 | 需额外关注含有高浓度空白脂质体制剂血浆的基质效性 | 无额外增加 |
回收率 | 低、高质控样本回收率 | 无额外增加 | 需额外关注不影响低、高质控样本准确度的最高空白脂质体制剂浓度 | 无额外增加 |
稳定性 | betch-top、反复冻融、长期储存和处理后上清放置稳定性 | 无额外增加 | 需额外关注脂质体存在下,经过储存、冻融时对游离化合物浓度的影响 | 无额外增加 |
由于脂质体类药物给药后,样本中既包含待测物,又有制剂存在,因此在模拟生物样本制备验证考察项时,需要关注空白制剂带来的影响。可以采用含空白脂质体(推荐选择总药ULOQ浓度下的空白制剂含量,或者是游离药物被洗脱的最大空白脂质体制剂浓度)的血浆基质,用于选择性和基质效应的考察。
脂质体制剂的特殊组分导致其脂质体表面易吸附疏水性化合物。采用SPE方法进行分离时,脂质体也可能存在与色谱柱固定相竞争吸附疏水性化合物,使得部分游离药物在上样的过程随着脂质体一起被带入负载型收集液中,从而产生游离型药物的低、高浓度回收率不一致的情况。因此,在方法开发过程中需要考察在空白脂质体存在下游离型药物的回收率,同时关注引起游离药物被洗脱的最大空白脂质体制剂浓度考察。在给药后的血浆样本的检测过程中,应将含有高浓度脂质体样本(高于考察最大浓度的脂质体样本)稀释到合适的浓度范围进行检测。
稳定性考察方面,既要考虑到游离型药物在基质中不同温度下的稳定性,又需要关注添加剂(稳定剂、抗凝剂等)的引入是否会引起脂质体结构的破坏。对此,在单独考量游离型药物物稳定性条件下,还需要关注脂质体在当前条件下的稳定性,以防出现因脂质体少量渗漏引起游离型药物稳定的“假阳性”定论。
离心转速
对于冻干粉脂质体制剂,溶解后一般为悬浊液,给药后需要采集的全血样本,放置一段时间后可能会发生分层现象,在离心制备血浆样本过程中可能存在脂质体在血浆中分布不均一的现象。因此需要考察离心力对脂质体分层和渗漏的影响。
可通过对于不同离心力下血浆中脂质体和游离药物的峰面积的差异测定来判定脂质体的均一性是否受到影响,从而选择合适的离心力进行血浆样本的制备。
另外,脂质体可能在涡旋混合的过程中发生渗漏,因此在制剂的配制过程中需要轻缓,尽可能低转速混合样本及工作液。
DMPK当前分析经验
药明康德药物代谢与动力学部(DMPK)当前已经通过以SPE法和超滤法两种前处理方式,完成了氟尿苷、盐酸伊立替康、紫杉醇、两性霉素B、瑞舒伐他汀等多个脂质体临床前体内药代动力学研究及新药申报工作。具备丰富的脂质体药物研究经验,也希望能为更多的脂质体药物研究赋能,服务于更多的制药公司和研发机构,缩短研发周期、加快药物上市、造福更多的病患。

图5. 脂质体药物分析相关主要耗材及仪器
结语
脂质体制剂组分复杂,不同的表面修饰在体内的理化性质有显著差异,因此在生物分析方法建立过程中的考量因素仍需“因药而异”。但总归离不开一个原则,即找到合适的分离方式进行游离型和负载型药物的分离,且需要确保脂质体从采集到处理的过程中保持状态稳定、不影响游离药物检测。
作者:安培云,卢金莲,邢丽丽
编辑:方健,钱卉娟
设计:倪德伟
药明康德DMPK依托中国(上海、苏州、南京和南通)和美国(新泽西)的研发中心,提供从早期筛选、临床前开发、到临床研究阶段的综合型药代动力学服务,助力您快速推进药物研发流程。拥有上千人的研发团队,服务超1600家全球客户,具有超过十五年的新药申报经验,已成功支持超过1700个新药临床研究申请(IND)。
点击此处与我们的专家进行联系
参考
[1] Hamdi Nsairat, Dima Khater, Usama Sayed, Fadwa Odeh, Abeer Al Bawab, Walhan Alshaer, Liposomes: structure, composition, types, and clinical applications, Heliyon 8 (2022) e09394.
[2] Pran Kishore Deb, Omar Al-Attraqchi, Balakumar Chandrasekaran, Anant Paradkar and Rakesh K. Tekade, Protein/Peptide Drug Delivery Systems: Practical Considerations in Pharmaceutical Product Development, Basic Fundamentals of Drug Delivery, 2019 (Pages 651-684).
[3] 《纳米药物非临床药代动力学研究技术指导原则》,2021年8月。
加入订阅
获取药物代谢与药代动力学最新专业内容和信息