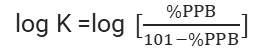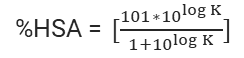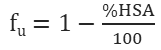在药物血浆蛋白结合(plasma protein binding, PPB)实验中,游离分数(fraction unbound, fu)是一个需要被准确测定的关键参数,该参数对预测药物相互作用(DDI)、评估治疗指数(TI)以及建立药代动力学/药效动力学(PK/PD)关系具有重要的作用[1]。目前,药物在血浆中fu的测定方法主要包括平衡透析法(equilibrium dialysis, ED)、超速离心法(ultracentrifugation, UC)、超滤法(ultrafiltration, UF)等,然而,对于某些高亲脂性、血浆稳定性较差或易发生非特异性吸附的化合物,传统方法常因半透膜吸附、孵育时间过长或离心过程中的药物降解,导致回收率不足,加之所测药物在血浆中溶解度较低,使得fu的准确测定面临挑战[2,3](如表1所示)。此外,对高蛋白结合药物而言,游离端药物浓度的检测对分析方法的灵敏度提出了极高要求。本文将介绍一种基于仿生色谱技术测定fu的新方法——HSA仿生色谱法,并系统阐述其基本原理、模型构建、验证过程与实际应用场景,以应对部分难以准确测定fu的化合物所面临的挑战。
表1. 药物血浆蛋白结合率的常用测定方法
类别 | 优点 | 局限性 |
平衡透析(ED) | %PPB测定的金标准 |
|
超滤法(UF) | 实验时间短,适用于不稳定化合物 |
|
超速离心法(UC) | 无膜参与,减少非特异性吸附 |
|
HSA仿生色谱法的介绍
仿生色谱是一种模拟人体生理环境的色谱技术,其核心在于使用仿生固定相(如磷脂、蛋白质、细胞膜组分等)作为分离介质。相较于传统色谱,仿生色谱能更真实地反映体内药物与生物相关成分之间的相互作用,为预测药物在体内的药代动力学行为提供有力支持[4]。
传统和商业上可用的仿生固定相包括人血清白蛋白(human serum albumin, HSA)、α1-酸性糖蛋白(α1-acid glycoprotein, AGP)以及固定化人工膜(immobilized artificial membrane,IAM)。这些固定相已被证明在早期药物研发方面具有重要的价值。在过去二十年里,许多用于预测分布容积、组织分配、蛋白结合及血脑屏障分布的模型相继发表。该方法已被包括GSK在内的多家制药公司应用于数十万种化合物的研究[4,5]。
HSA作为人体血浆中含量最丰富的蛋白质(约占血浆总蛋白的55%),是药物血浆蛋白结合的重要载体,尤其对酸性、中性及部分碱性药物表现出较高的结合亲和力。基于其在血浆中的高丰度及广泛的结合特性,本研究将重点围绕HSA仿生色谱法展开[6]。
原理
HSA仿生色谱法,即在高效液相色谱系统中采用键合HSA的固定相,模拟药物在体内的蛋白结合环境。当待测物在模拟生理条件(如pH7.4 缓冲液)的流动相中流经色谱柱时,其与固定相HSA之间的结合-解离动力学决定了其在柱上的保留行为(如图1所示)。通常,与HSA结合能力越强的分子,在HSA色谱柱上的保留时间越长,反之则越短[7]。通过建立药物在该仿生色谱体系中的保留时间与血浆蛋白结合率(%PPB)之间的相关模型,即可利用简便、快速的色谱实验预测药物在体内的血浆蛋白结合程度,并由此推算出游离分数(fu)。
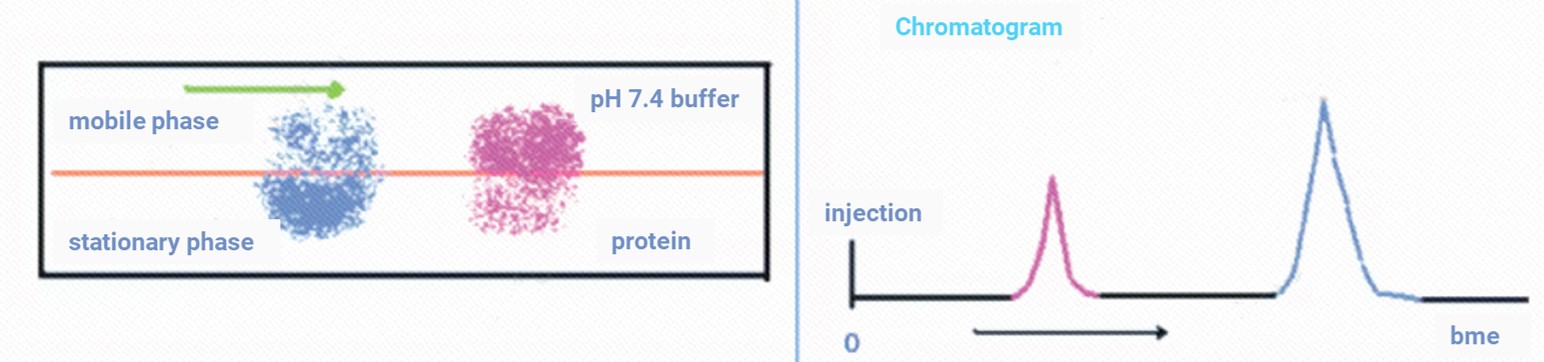
图1. 化合物保留行为受流动相与固定相的相互作用影响
方法
该方法无需在血浆中孵育。具体操作如下:将待测物储备液用醋酸铵溶液(pH 7.4)与异丙醇的混合溶液稀释至适当浓度,充分混匀后,进行LC-MS/MS分析,测定化合物在仿生色谱柱上的保留时间(retention time, tR)。
表2. HSA仿生色谱法中%PPB的计算方程[8]
Equation.1 |
|
Equation.2 |
|
Equation.3 |
|
模型建立与验证
研究选取了10种市售化合物,其人血浆蛋白结合率(%PPB)覆盖5%至99.5%,分为低、中、高结合率三类。结果显示,化合物的保留时间与文献报道的血浆蛋白结合率之间呈显著线性相关,相关系数R2为0.9923(如图2所示)。
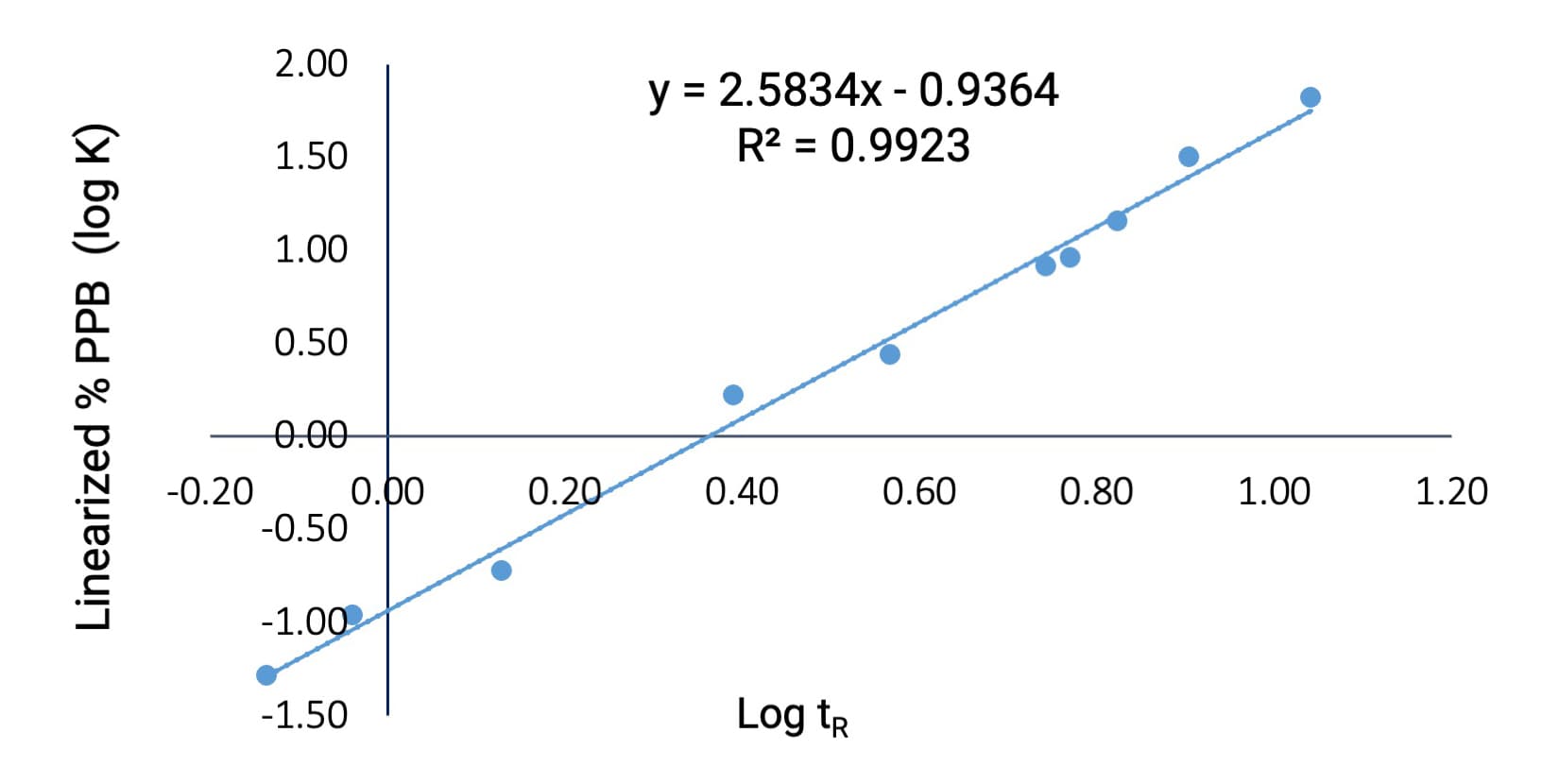
图2. 保留时间与蛋白结合率之间的相关性
HSA仿生色谱法的特点
相较于传统的平衡透析法、超速离心法及超滤法,HSA仿生色谱法在评估药物血浆蛋白结合方面具有以下特点:
应当指出,文献通常报道的是血浆蛋白结合率,而我们的实测数据仅反映化合物与人血清白蛋白(HSA)的结合率。尽管如此,两者之间存在着可接受的相关性,因此该方法仍可在早期药物发现阶段用于化合物筛选工作。KLARA VALKO等人在其发表的文章中也印证了这一相关性[9]。
HSA仿生色谱法在药物血浆蛋白结合研究中的应用
典型案例如下:
案例1 不稳定小分子药物——卡托普利
卡托普利是一种临床常用的降压及心力衰竭治疗药物,其分子中的巯基易发生氧化,可与自身或血浆中的内源性含巯基化合物(如半胱氨酸、谷胱甘肽)发生反应,导致稳定性较差。在传统的血浆蛋白结合实验中,该特性常引起回收率偏低,影响游离分数测定的准确性。传统方法通常需额外优化还原体系(如TCEP等)以确保fu结果的可靠性,而仿生色谱法无需血浆孵育,可有效避免此类稳定性问题。经验证,该方法测得的fu值与在人血浆超滤法结果较为接近(如表3所示)。
表3. 卡托普利血浆游离分数不同测定方法的比较
化合物 | 游离分数(fu) | |
超滤法 | HSA仿生色谱法 | |
卡托普利 | 0.8310 | 0.9365 |
案例2 易发生非特异性吸附药物——帕瑞肽
帕瑞肽是一种用于治疗库欣病与肢端肥大症的孤儿药,其分子结构为含有14个氨基酸的环肽。在实验过程中易发生非特异性吸附,导致样品前处理时提取回收率低;同时,帕瑞肽具有较高的血浆蛋白结合率,对分析方法灵敏度提出较大挑战。采用仿生色谱法进行测定,所得fu与在人血浆超速离心法的测定结果高度一致(如表4所示),有效避免了吸附损失与灵敏度不足带来的误差。
表4. 帕瑞肽血浆游离分数不同测定方法的比较
化合物 | 游离分数(fu) | |
超速离心法 | HSA仿生色谱法 | |
帕瑞肽 | 0.0307 | 0.0294 |
结语
在药明康德DMPK,我们所建立的HSA仿生色谱法已成功应用于近百个分子的血浆蛋白结合率评估。除传统小分子药物外,该方法也适用于多肽等部分新分子实体,并能有效应对基质稳定性差或非特异性吸附强等挑战性场景。因此,该平台可作为fu测定的一项差异化补充策略。
药明康德DMPK具备全面的血浆蛋白结合(PPB)测定技术体系,涵盖平衡透析法(包括HTD和RED)、超速离心法、超滤法、通量透析法、竞争透析法、仿生色谱法以及报告酶法(用于动态蛋白结合研究)。我们可在血浆、组织匀浆、肝细胞、肝微粒体等多种生物基质中开展蛋白结合实验,并能支持各类复杂性质化合物的测试,包括不稳定化合物、高结合率化合物、共价抑制剂、多肽、TPD、siRNA、ASO等,为药物研发提供多方位、高灵活性的支持。
作者:李敏霞、陆春红、孙梦洁、文欣欣、王洁、李小童、邢丽丽
编辑:富罗娜·克里木、钱卉娟
设计:张莹莹
药明康德DMPK依托中国(上海、苏州、南京和南通)和美国(新泽西)的研发中心,提供从早期筛选、临床前开发、到临床研究阶段的综合型药代动力学服务,助力您快速推进药物研发流程。拥有上千人的研发团队,服务超1600家全球客户,具有超过十五年的新药申报经验,已成功支持超过1700个新药临床研究申请(IND)。
点击此处与我们的专家进行联系
参考
[1] Di Li. An update on the importance of plasma protein binding in drug discovery and development, Expert Opinion on Drug Discovery, 2021, 16(12): 1453–1465.
[2] Dunja Dimitrijevic, Eric Fabian, Dorothee Funk-Weyer, Robert Landsiedel. Rapid equilibrium dialysis, ultrafiltration or ultracentrifugation? Evaluation of methods to quantify the unbound fraction of substances in plasma, Biochemical and Biophysical Research Communications, 2023, 651: 114–120.
[3] Brigitte Buscher, Sirpa Laakso, Hermann Mascher, Klaus Pusecker, Mira Doig, Lieve Dillen, Winfried Wagner-Redeker, Thomas Pfeifer, Pascal Delrat, Philip Timmerman. Bioanalysis for plasma protein binding studies in drug discovery and drug development: views and recommendations of the European Bioanalysis Forum, Bioanalysis, 2014, 6(5): 673–682.
[4] Klara Valkó. Biomimetic chromatography—A novel application of the chromatographic principles, Analytical Science Advances, 2022, 3: 146–153.
[5] Shenaz Bunally,Robert J. Young. The role and impact of high throughput biomimetic measurements in drug discovery. ADMET & DMPK, 2018 6(2): 74-84.
[6] George Lambrinidis, Theodosia Vallianatou, Anna Tsantili-Kakoulidou. In vitro, in silico and integrated strategies for the estimation of plasma protein binding: A review, Journal of Pharmaceutical and Biomedical Analysis, 2015, 86: 27–45.
[7] Klara Valkó. Biomimetic chromatography to accelerate drug discovery: Part 1, LCGC North America, 2018, 36.
[8] Klara Valkó, Shenaz B Nunhuck, Alan P Hill. Estimating unbound volume of distribution and tissue binding by in vitro HPLC-based human serum albumin and immobilised artificial membrane-binding measurements, Journal of Pharmaceutical Sciences, 2011, 100(3): 123–130.
[9] Klara Valkó, Shenaz Nunhuck, Chris Bevan, Michael H. Abraham, Derek P. Reynolds. Fast Gradient HPLC Method to Determine Compounds Binding to Human Serum Albumin. Relationships with Octanol/Water and Immobilized Artificial Membrane Lipophilicity. Journal of Pharmaceutical Sciences, 2003, 92(11): 2236–2248.
加入订阅
获取药物代谢与药代动力学最新专业内容和信息