淋巴系统的研究对于治疗淋巴类疾病的药物,以及利用淋巴吸收途径促进吸收的药物均有着至关重要的作用[1]。药物经淋巴吸收的优势在于直接将药物输送到免疫系统,无需经过肝首过代谢。近年来,淋巴系统的相关生物学靶标越来越多地被发现和利用,药物经由淋巴循环的吸收、分布、转运与代谢过程及相关的递送系统也引起了广泛关注。本文将阐述不同分子大小的药物在体内经由淋巴转运吸收的机理及体内外研究模型,重点介绍大鼠淋巴插管模型的建立及应用。
淋巴系统与淋巴循环
淋巴系统是人体免疫防御系统的重要组成部分,主要由淋巴管(如毛细淋巴管、淋巴干和淋巴导管)、淋巴组织(如弥散淋巴组织和淋巴结)和淋巴器官(如胸腺、骨髓和扁桃体等)构成(如图1所示)[2]。人体的淋巴系统网与血管网交织伴行,两者共同组成人体循环系统。与血管系统不同,淋巴系统是一个开放式的回路,组织液通过组织内的淋巴毛细血管进入淋巴管,这些毛细血管流经更大的前收集淋巴管后进入淋巴结,最终淋巴管在胸淋巴管(乳糜池)或右淋巴管汇合,将淋巴管汇入锁骨下静脉的血液循环中。因此,淋巴系统在维持体液平衡、清除细胞碎片和体内有毒废物、调节免疫以及将脂质(以白蛋白的形式)从组织转运到血液循环中发挥重要的生理功能[3, 4]。
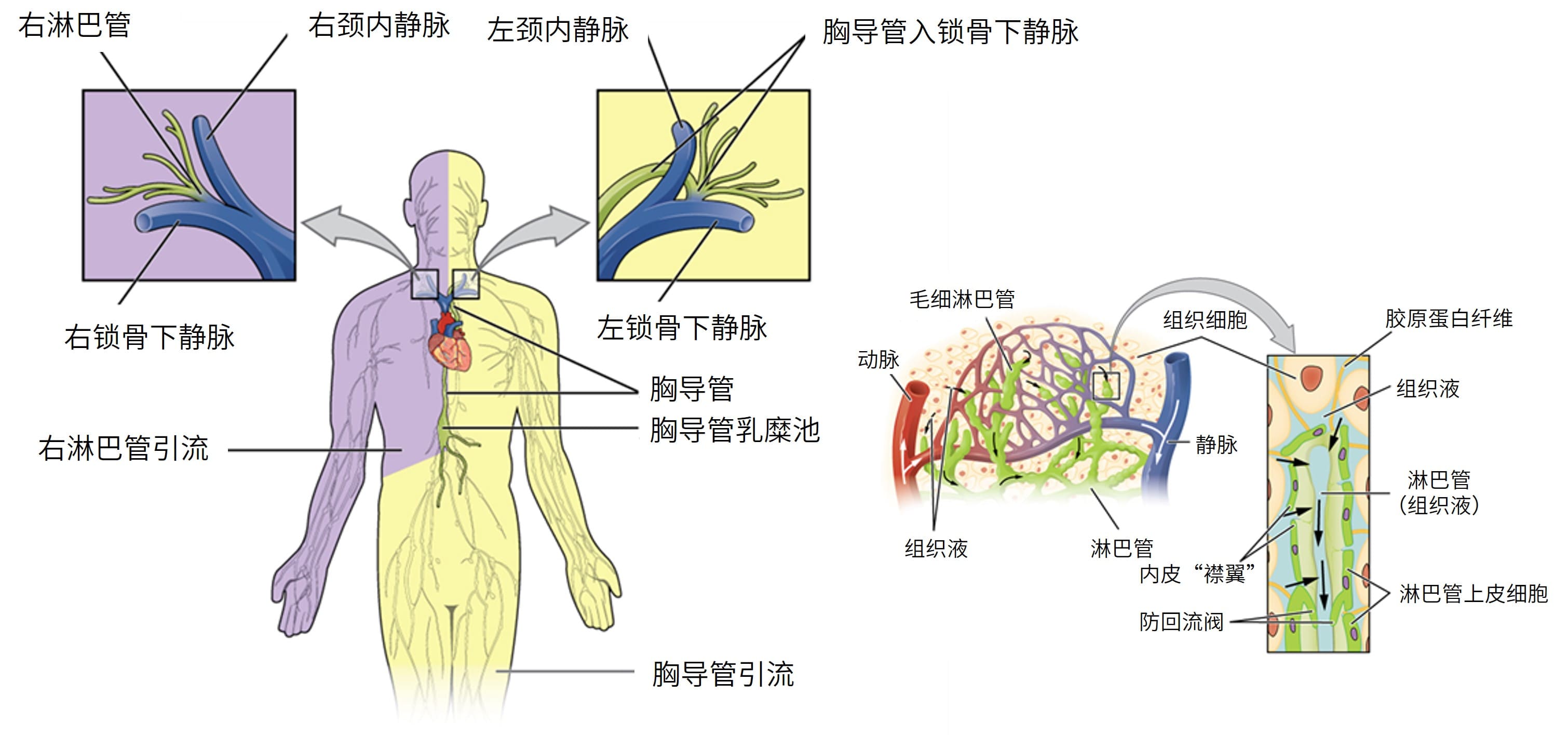
图1. 淋巴系统的主干与导管及组织间隙毛细淋巴管局部放大图[5]
药物经淋巴转运递送
毛细血管和淋巴管具有不同的生理结构,对化合物的通透性也有差异,致使大分子和小分子药物在淋巴液和血液中的转运表现出显著区别。通常情况下,小分子药物可以自由地在血管和淋巴管内被吸收和转运,但血液量是淋巴液流量的100-500倍,导致在血液内容易产生较强的漏槽条件,而大多数药物通过引流毛细血管从组织和给药部位清除。因此,小分子药物更易于在血液内转运和吸收[6, 7]。然而对于大分子药物(分子量大于20 KDa或分子直径为10-100 nm的大分子),因其分子结构过大无法顺利穿过毛细血管内皮,所以更易于在淋巴管内转运。大分子(或高脂溶性)药物通过与肠上皮细胞上的脂蛋白结合,经肠系膜淋巴管进入体循环,可以有效地避免肝首过效应。关于大分子药物在体内的转运及吸收情况,研究人员不但探究大分子药物在淋巴循环过程中的药代动力学过程,而且利用大分子为载体助力小分子药物进入淋巴系统,增加药物在目标靶位置的释放,从而增加药物在体内的暴露量。
药物经肠淋巴转运与经门静脉吸收相比的优点包括:
肠淋巴转运可有效避免肝首过[8];
制剂处方的调整可影响高脂溶性化合物转运及药动学参数,有助于药物治疗及毒理学的评价[9];
淋巴系统是T和B淋巴细胞及肿瘤扩散的主要通道,可提高淋巴靶向药物的药效[10]。
药物经淋巴转运的研究模型
体外模型
Caco-2细胞模型是目前应用较为广泛的一种研究淋巴转运的体外模型,由于其可以分泌脂蛋白(TRLs),并提供细胞水平上的机制研究,被用于评价药物在肠淋巴转运及脂质和相关辅料对于药物与脂蛋白结合的影响,是鉴定肠淋巴运输候选药物的有效工具之一[11]。Seeballuck等[12]使用Caco-2模型研究表面活性剂聚山梨酸60和聚山梨酸80对小肠分泌脂蛋白的影响,研究表明Caco-2细胞消化聚山梨酸80释放油酸,油酸被细胞用来促进富含甘油三酯的脂蛋白(包括乳糜微粒)的基底外侧分泌。聚山梨酯80在体内大鼠模型中引起了类似的反应,刺激肠系膜淋巴中甘油三酯分泌增加;而聚山梨酯60却未出现类似的反应。
体内模型
药物在淋巴系统内转运的体内评价一直是该研究的难点之一。评估药物在淋巴转运需要进行淋巴管插管来直接测定淋巴内药物的浓度,但淋巴插管属于非可逆手术,药物在淋巴转运研究不能在人体内进行。因此,研究者建立了各种动物模型用来定量描述药物在淋巴的转运。淋巴插管的动物模型收集流入肠系膜或胸腔淋巴管中的淋巴液,通过不同时间段内收集的淋巴液体积与浓度的乘积获得药物在淋巴的转运量。1948年Bollman等人首次建立了大鼠肠系膜淋巴液引流技术[13],促进了许多研究的开展。然而该类手术难度高、成功率较低,且动物处于麻醉或受限制的状态下,无法模拟动物正常生理状态下的淋巴转运情况。目前,大鼠淋巴插管模型是最常用的淋巴转运研究模型之一(如图2所示),麻醉与清醒大鼠的淋巴转运模型各有优缺点,如表1所示。
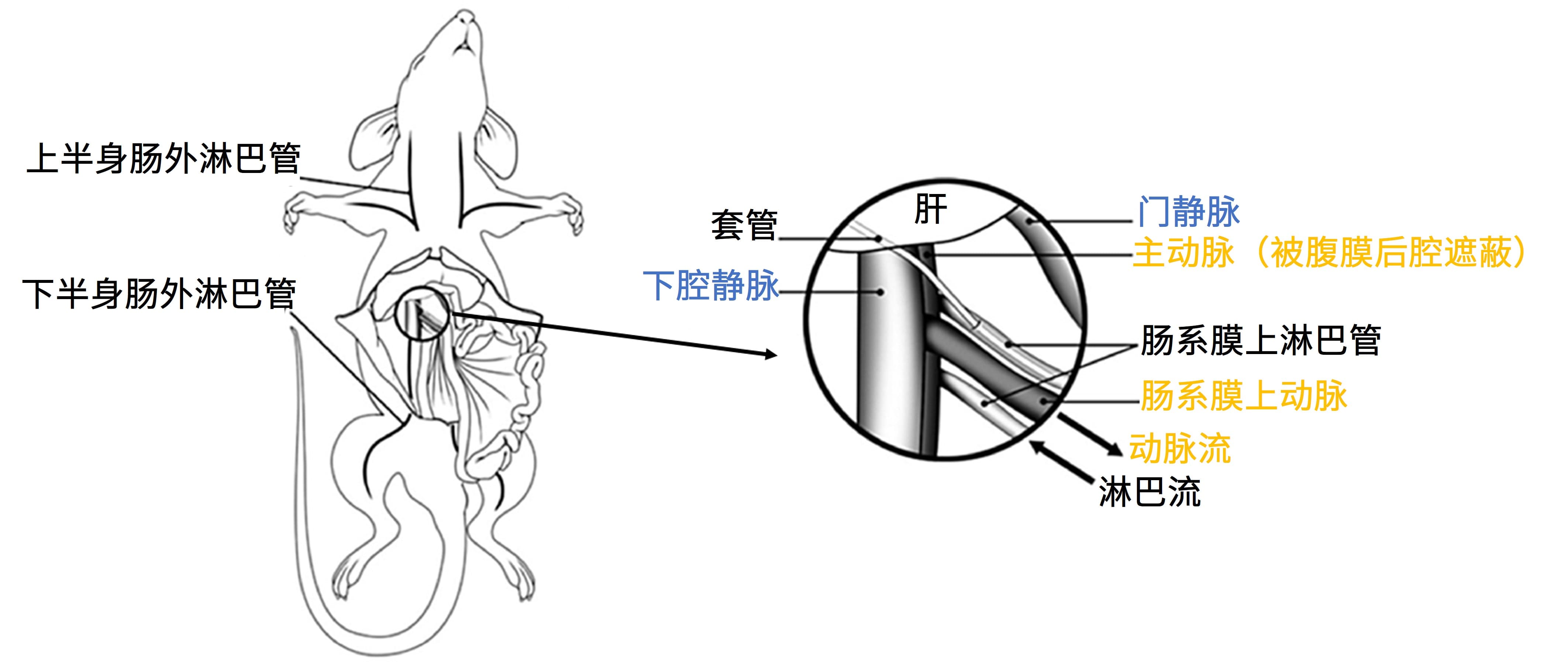
图2. 大鼠肠系膜淋巴管插管模型图[14]
表1. 麻醉与清醒*大鼠淋巴转运模型对比
动物模型 | 给药方式 | 手术类型 | 实验时长 | 优缺点 |
麻醉 | 十二指肠 | 肠系膜淋巴管/胸导管插管 | ≤8小时 |
|
清醒 | 口服 | 肠系膜淋巴管/胸导管插管 | ≤6天 |
|
*可自由活动的大鼠
药明康德DMPK现已搭建大鼠淋巴吸收相关研究模型(解读丨大鼠肠系膜淋巴管插管模型验证渗透性增强剂SNAC对淋巴吸收的影响)。以维生素D3和盐酸卤泛群(高脂溶性化合物)为待测药物[15-19],评估麻醉与否对淋巴转运情况的影响,以及不同的淋巴液收集位置对淋巴转运相关PK研究的影响,实验设计如表2所示。
表2. 麻醉与非麻醉大鼠淋巴转运模型验证实验设计
实验分类 | 组别 | 动物品系 | 麻醉与否(Y/N) | 给药方式 | 待测药物 | 手术方式 | 样本收集 | |
血样(Y/N) | 淋巴液(Y/N) | |||||||
A | 1 | SD Rat/Male | Y | 十二指肠 | 维生素D3 | 肠系膜插管 | N | Y |
2 | SD Rat/Male | N | 口服 | N | Y | |||
B | 3 | SD Rat/Male | N | 口服 | 盐酸卤泛群 | 胸导管 | Y | Y |
4 | SD Rat/Male | N | 口服 | 肠系膜插管 | Y | Y | ||
5 | SD Rat/Male | N | 口服 | 门静脉插管 | Y | N | ||
6 | SD Rat/Male | N | 口服 | 非手术 | Y | N | ||
表3.维生素D3在麻醉与清醒动物模型下淋巴液中相关PK参数[15]
药物在淋巴液中的总回收率(%/8h) | 淋巴液流速(µL/8h) | 假手术组血样中AUC 0-8h(µg·h/mL)** | |
麻醉 | 9 ± 1.5 | 2461.2 ± 1028.4 | 4.8 ± 0.7 |
清醒 | 12 ± 1.8 | 7366.6 ± 1501.9 | 6.5 ± 0.9 |
**肠系膜淋巴管假手术,即麻醉动物开腹后,暴露肠系膜淋巴管,静置30分钟
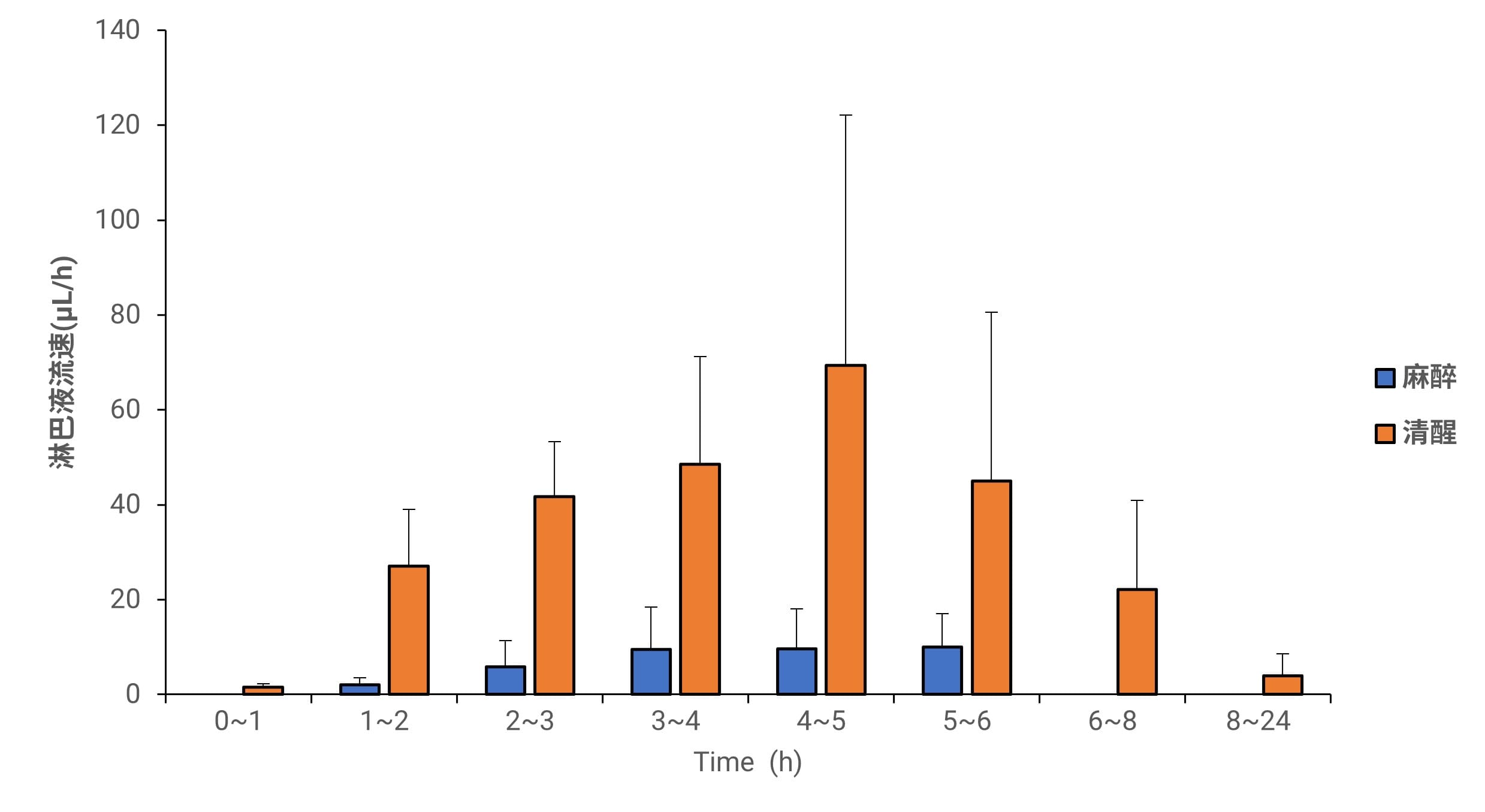
图3. 维生素D3在麻醉与清醒动物模型淋巴液中的流速,数据以Mean ± SD表示(n=4)
表4. 维生素D3在麻醉与清醒动物模型下淋巴液中相关PK参数
药物总回收量(µg) | 药物在淋巴液中的总回收率(%/6h) | 淋巴液流速(µL/6h) | |
麻醉 | 37.1 ± 31.0 | 3.20 ± 2.1 | 3597 ± 1564 |
清醒 | 341 ± 179 | 13.0 ± 3.3 | 12644 ± 4.85 |
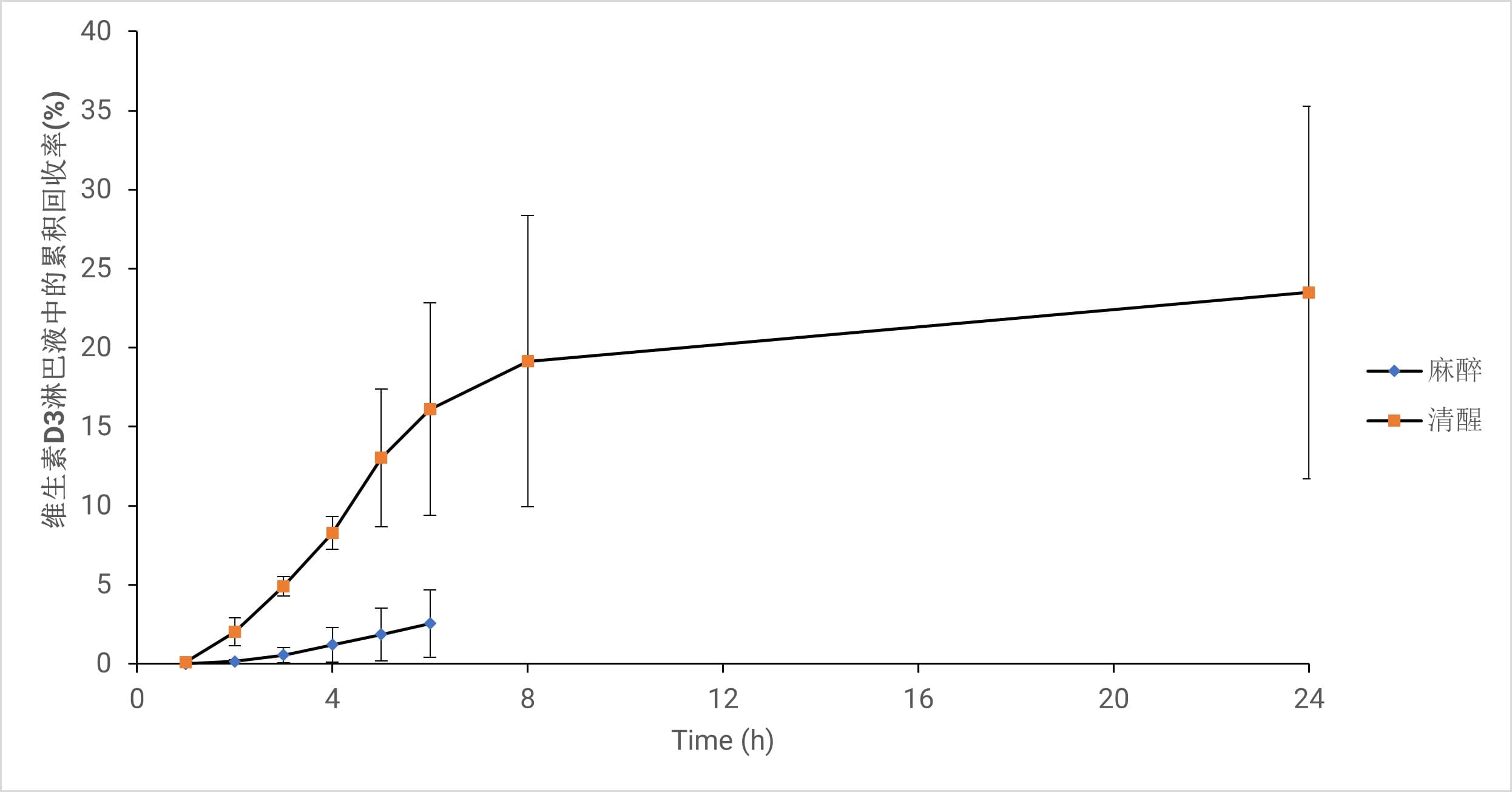
图4. 维生素D3在麻醉与清醒动物模型淋巴液中的累积回收率,数据以Mean ± SD表示(n=4)
研究表明在不同实验模型中,维生素D3的运输途径并未受到麻醉的阻碍,假手术组维生素D3在清醒和麻醉状态下血浆中(维生素D3通过淋巴途径与非淋巴途径吸收的药物总量)的AUC0-8h值分别为6.5和4.8 (µg·h/mL)(如表3所示)。与此同时,维生素D3在清醒与麻醉状态下淋巴转运均呈现连续状态,在给药8h后,清醒组和麻醉组通过淋巴运输的剂量分别约为给药剂量的12%和9%。麻醉组相较于清醒组的维生素D3的淋巴转运量下降约25% [15]。尽管由于麻醉导致维生素D3的吸收总量有所减少,但药物的吸收模式并未发生改变,因此,涉及不同吸收途径的生理过程没有受到严重阻碍。
此外,使用麻醉大鼠模型,不仅可以简化手术过程、加快手术速度,还可以节省动物术后恢复时间。与此同时,与清醒大鼠模型相比,麻醉大鼠模型可维持淋巴插管通畅率和减少术后脱管发生率。因此,对于口服经淋巴吸收药物的快速筛选,可将麻醉动物模型作为优选,而对于探索特定分子的吸收特性,清醒动物模型可能更合适。
表5. 盐酸卤泛群在不同实验模型下血浆的相关PK参数
PK参数 | 胸导管 | 肠系膜淋巴管 | 门静脉插管 | 非手术 |
Cmax (ng/mL) | 161.5 ± 43.2 | 183 ± 49.0 | 453 ± 227 | 383 ± 192 |
Tmax (h) | 20 ± 8.00 | 16.0 ± 9.24 | 8.00 ± 0.00 | 12.0 ± 8.00 |
T1/2 (h) | 36.7 ± 17.9 | 30.5 ± 2.67 | 64.1 ± 93.8 | 66.7 ± 19.0 |
AUC0-inf (ng.h/mL) | 11194.5 ± 5968 | 7083 ± 1908 | 21247 ± 10794 | 18815 ± 5249 |
MRT0-inf (h) | 61.8 ± 24.5 | 45.6 ± 6.68 | 77.6 ± 49.6 | 79.6 ± 14.7 |
Hepatic Extraction ratio | N/A | N/A | 0.120 ± 0.106 | N/A |
表6. 盐酸卤泛群在不同实验模型下淋巴液中的回收率
肠系膜淋巴管 | 胸导管 | |
药物总回收量(ng) | 261917 ± 86024.78 | 531402 ± 107797.79 |
药物在淋巴液中的总回收率(%) | 11 ± 3.42 | 23 ± 4.76 |
淋巴清除率(mL/min/kg) | 2 ± 1.11 | 4 ± 1.50 |
实验结果表明,不同的淋巴收集部位对经淋巴吸收的药物评价会有所影响。其中,肠系膜淋巴插管主要收集下半身和肠淋巴吸收的药物,胸导管主要收集间质间隙毛细血管收集的药物,约占体内淋巴循环的四分之三(如表5所示)。不同的实验模型对淋巴循环研究范围的差异,导致对药物经淋巴循环的相关PK参数的评价会略有不同。因此,在实验开展过程中,结合不同的实验目的选择匹配的实验模型才能获得更加准确的实验结果反馈。
结语
药物经淋巴转运吸收可以避免肝首过代谢作用,从而增加口服药物的生物利用度,对于具有强首过代谢的药物,淋巴转运途径具有重要的意义,尤其对于高亲脂难溶性药物的开发和利用表现出巨大的潜力。药明康德DMPK已经成功搭建了大鼠淋巴吸收的相关研究模型,助力经淋巴吸收途径的药物的药代动力学等相关研究。
作者:焦桴荣,董轩,陈运喜,马红磊,汤城
编辑:富罗娜·克里木,钱卉娟
设计:倪德伟,张莹莹
药明康德DMPK依托中国(上海、苏州、南京和南通)和美国(新泽西)的研发中心,提供从早期筛选、临床前开发、到临床研究阶段的综合型药代动力学服务,助力您快速推进药物研发流程。拥有上千人的研发团队,服务超1600家全球客户,具有超过十五年的新药申报经验,已成功支持超过1700个新药临床研究申请(IND)。
点击此处与我们的专家进行联系
参考
[1] Abdallah M, Müllertz OO, Styles IK, et al. Lymphatic targeting by albumin-hitchhiking: Applications and optimisation. J Control Release. 2020;327:117-128.
[2] Moore JE Jr, Bertram CD. Lymphatic System Flows. Annu Rev Fluid Mech. 2018;50:459-482.
[3] Trevaskis NL, Kaminskas LM, Porter CJ. From sewer to saviour - targeting the lymphatic system to promote drug exposure and activity. Nat Rev Drug Discov. 2015;14(11):781-803.
[4] Sweeney MD, Zlokovic BV. A lymphatic waste-disposal system implicated in Alzheimer's disease. Nature. 2018;560(7717):172-174.
[5] Anatomy of the Lymphatic and Immune Systems.Anatomy and Physiology | OpenStax
[6] Chakraborty S, Shukla D, Mishra B, Singh S. Lipid--an emerging platform for oral delivery of drugs with poor bioavailability. Eur J Pharm Biopharm. 2009;73(1):1-15.
[7] 柴旭煜,陶涛.脂质促进药物经肠淋巴转运的研究进展[J].中国药学杂志, 2008, 43(22):4.
[8] Trevaskis NL, Charman WN, Porter CJ. Lipid-based delivery systems and intestinal lymphatic drug transport: a mechanistic update. Adv Drug Deliv Rev. 2008;60(6):702-716.
[9] Caliph SM, Trevaskis NL, Charman WN, Porter CJ. Intravenous dosing conditions may affect systemic clearance for highly lipophilic drugs: implications for lymphatic transport and absolute bioavailability studies. J Pharm Sci. 2012;101(9):3540-3546.
[10] Cense HA, van Eijck CH, Tilanus HW. New insights in the lymphatic spread of oesophageal cancer and its implications for the extent of surgical resection. Best Pract Res Clin Gastroenterol. 2006;20(5):893-906.
[11] Karpf DM, Holm R, Garafalo C, Levy E, Jacobsen J, Müllertz A. Effect of different surfactants in biorelevant medium on the secretion of a lipophilic compound in lipoproteins using Caco-2 cell culture. J Pharm Sci. 2006;95(1):45-55.
[12] Seeballuck F, Lawless E, Ashford MB, O'Driscoll CM. Stimulation of triglyceride-rich lipoprotein secretion by polysorbate 80: in vitro and in vivo correlation using Caco-2 cells and a cannulated rat intestinal lymphatic model. Pharm Res. 2004;21(12):2320-2326.
[13] Kraft JC, Freeling JP, Wang Z, Ho RJ. Emerging research and clinical development trends of liposome and lipid nanoparticle drug delivery systems. J Pharm Sci. 2014;103(1):29-52.
[14] Banan B, Wei Y, Simo O, et al. Intestinal Lymph Collection via Cannulation of the Mesenteric Lymphatic Duct in Mice. J Surg Res. 2021;260:399-408.
[15] Dahan A, Mendelman A, Amsili S, Ezov N, Hoffman A. The effect of general anesthesia on the intestinal lymphatic transport of lipophilic drugs: comparison between anesthetized and freely moving conscious rat models. Eur J Pharm Sci. 2007;32(4-5):367-374.
[16] Brocks DR, Toni JW. Pharmacokinetics of halofantrine in the rat: stereoselectivity and interspecies comparisons. Biopharm Drug Dispos. 1999;20(3):165-169.
[17] Khoo SM, Prankerd RJ, Edwards GA, Porter CJ, Charman WN. A physicochemical basis for the extensive intestinal lymphatic transport of a poorly lipid soluble antimalarial, halofantrine hydrochloride, after postprandial administration to dogs. J Pharm Sci. 2002;91(3):647-659.
[18] Porter CJ, Charman SA, Charman WN. Lymphatic transport of halofantrine in the triple-cannulated anesthetized rat model: effect of lipid vehicle dispersion. J Pharm Sci. 1996;85(4):351-356.
[19] Porter CJ, Charman SA, Humberstone AJ, Charman WN. Lymphatic transport of halofantrine in the conscious rat when administered as either the free base or the hydrochloride salt: effect of lipid class and lipid vehicle dispersion. J Pharm Sci. 1996;85(4):357-361.
加入订阅
获取药物代谢与药代动力学最新专业内容和信息