随着偶联药物成为药物研发的热门领域,多肽偶联放射性核素药物(PRC)也进入了发展的黄金时代。2018年,首个放射性多肽靶向肿瘤治疗药物Lutathera(177Lu-Dotatate)的获批,标志着多肽偶联放射性核素药物(PRC)正式登上抗癌舞台。截至目前,全球范围内获批上市的PRC药物共计9款,其中诊断类药物7款,治疗类药物2款,即诺华的Lutathera®和Pluvicto®。放射性标记的奥曲肽衍生物已在神经内分泌肿瘤的常规核医学诊断与治疗中获得成功应用,体现出良好的临床转化潜力。此外,Bicycle Therapeutics plc近期公布了其首个人体成像数据,不仅验证了MT1-MMP作为癌症治疗新靶点的潜力,也展现出Bicycle放射性核素偶联物(BRC)在放射药物应用中的优势。本文将系统介绍PRC药物的结构特征、优势和代谢特性以及在代谢研究实验中的考量,以期为该类药物的研发提供参考思路。
表1. 已获批的多肽偶联放射性核素药物
药名 | 类别 | 生产厂家 | 靶点 | 适应症 | 获批时间 |
68Ga-PSMA-11 | 诊断 | 诺华 | PSMA | 前列腺癌 | 2022/3 |
lutetium Lu-177 vipivotide tetraxetan | 治疗 | 诺华 | PSMA | 去势抵抗性前列腺癌 | 2022/3 |
TLX591-CDx | 诊断 | Telix; 远大医药 | PSMA | 前列腺癌 | 2021/12 |
68Ga-PSMA-11 | 诊断 | University of California | PSMA | 前列腺癌 | 2020/12 |
铜[64Cu]-氧奥曲肽 | 诊断 | RadioMedix | SSTR2 | 神经内分泌肿瘤 | 2020/9 |
镓[68Ga]-依度曲肽 | 诊断 | Isotope Technologies Munich; 远大医药 | SSTR2 | 神经内分泌肿瘤 | 2019/8 |
177Lu-DOTATATE | 治疗 | 诺华 | SSTR2 | 胃肠胰神经内分泌肿瘤,神经内分泌肿瘤 | 2018/1 |
镓[68Ga]-依度曲肽 | 诊断 | 诺华 | SSTR2 | 胃肠胰神经内分泌肿瘤,神经内分泌肿瘤 | 2016/12 |
镓[68Ga]-氧奥曲肽 | 诊断 | 诺华 | SSTR2 | 神经内分泌肿瘤 | 2016/6 |
铟[111In]-喷曲肽 | 诊断 | Curium | SSTR2 | 神经内分泌肿瘤 | 1994/6 |
多肽偶联放射性核素药物(PRC)的结构
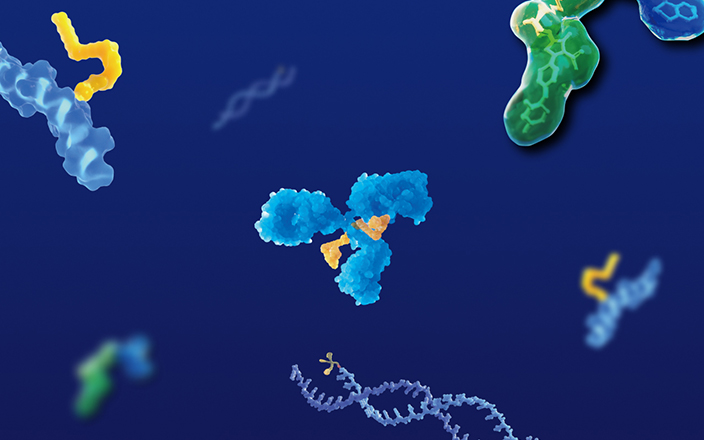
PRC的基本结构通常包括放射性核素和靶向多肽,或在此基础上引入螯合剂、连接子等辅助单元,形成更为复杂的偶联体系(图1)。与抗体偶联药物(ADC)相比,PRC最大的区别是载荷并非毒性小分子,而是具有诊断或治疗功能的放射性核素。放射性核素通过放射线发挥作用,无需进入细胞内部,其连接子也无需裂解释放活性载荷,从而增强了PRC在体内的安全性和稳定性。多肽部分则发挥精准定位作用,将放射性核素靶向递送至靶器官,进而实现诊疗一体化的功能。
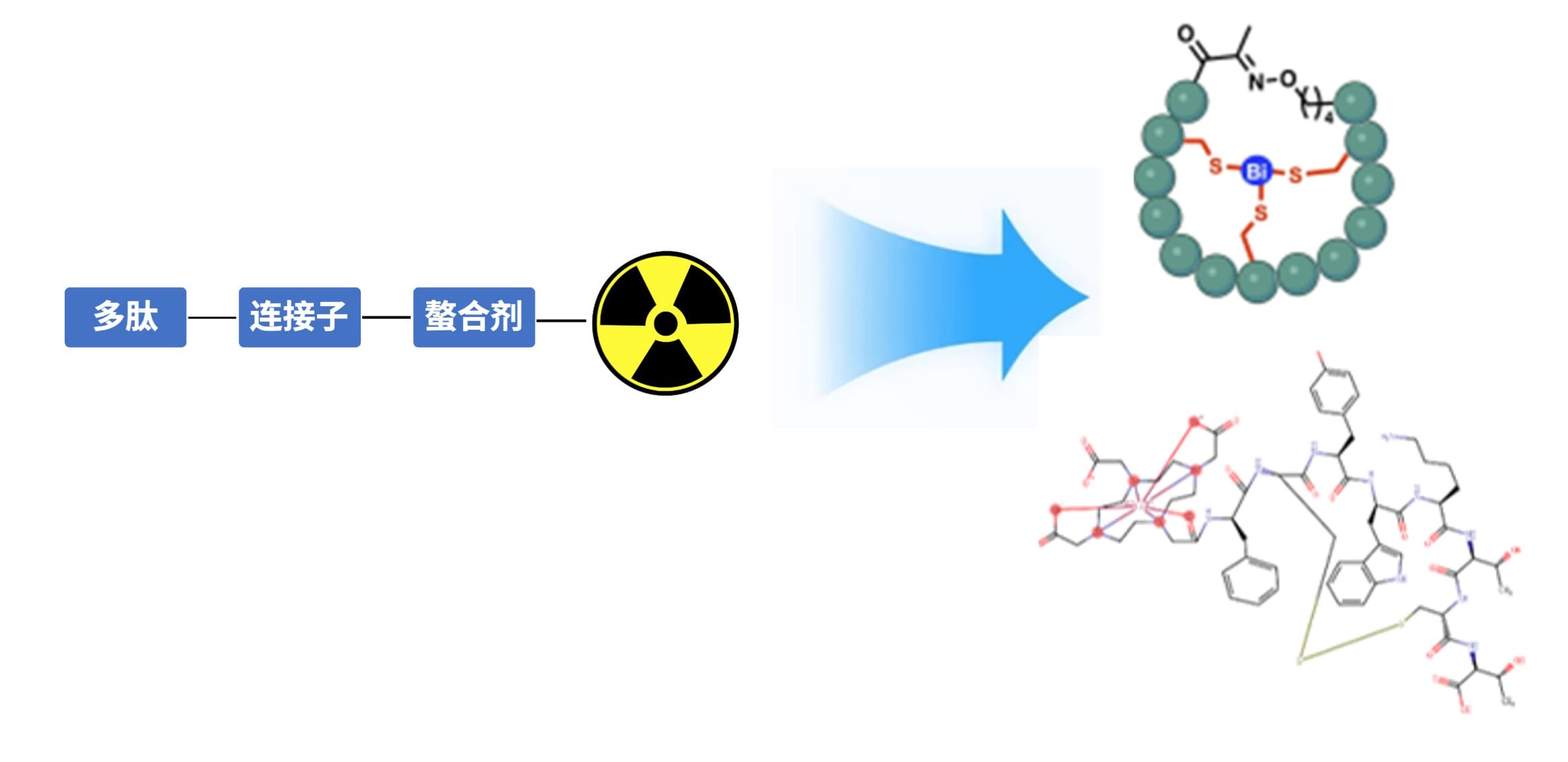
图1. 多肽偶联放射性核素药物(PRC)的结构示例
放射性核素
放射性核素通过衰变释放的α、β、γ射线,通过破坏肿瘤细胞DNA从而发挥治疗作用,其中穿透能力较强的射线也可用于成像诊断。目前已有30多种放射性核素被应用于疾病的诊断与治疗(如表2)。177Lu是目前PRC中最常用的诊疗一体化核素,可同时发射用于治疗的β粒子和用于显像的γ射线。225Ac是近年来进入临床的新型核素,主要释放α粒子,虽然其组织穿透性弱,但杀伤能力更强[1]。
表2. 不同放射性核素的特征总结
释放射线 | 组织中的射程 | DNA损伤 | 特点及应用 | 代表核素 |
α射线 | 50-100 μm | 导致DNA双链断裂,对细胞破坏性大、损伤复杂,修复困难 |
| 铋[213Bi]、铅[212Pb]、镭[223Ra]、锕[225Ac]、钍[227Th]、砹[211At] |
β射线 | 2-12 mm | 导致DNA单链/双链断裂,主要通过间接作用产生自由基来损伤DNA,相对容易修复 |
| 镥[177Lu]、碘[131I]、钇[90Y]、铜[67Cu]、铼[188Re] |
γ射线 | 低能量γ射线: 几毫米 中等能量γ射线: 几厘米 | 导致DNA单链/双链断裂,因为穿透力强,能造成多个位点的双键断裂,较难修复 |
| 镥[177Lu]、镓[67Ga]、锝[99mTc]、锶[131Sr] 、碘[125I] |
多肽
多肽通常由10至40个氨基酸组成,分子量一般小于10 kDa。可根据结构分为天然氨基酸组成的线性肽、含有非天然氨基酸结构的线性肽以及环肽等类型。
多肽药物兼具小分子药物与蛋白质类药物的优点,主要体现在以下几个方面:
靶向性强、特异性高:多肽能够以高亲和力结合特定受体,副作用较低。例如,放射性标记的蛙皮素类似物可精准靶向肿瘤细胞中过度表达的GRPR,用于前列腺癌的早期诊断与治疗。
免疫原性低、组织穿透能力强。
代谢特性优良:多肽由氨基酸构成,其代谢产物为氨基酸,通常无毒副作用。
稳定性可通过结构优化提升:线性肽构象较为灵活,易被蛋白酶降解。通过环化策略可限制其构象柔性,增强结构稳定性,减少因外肽酶催化引起的代谢降解,降低解离常数,提高靶点亲和力。因此,一般选择环肽作为PRC药物的配体,从而提升PRC药物的体内稳定性与药效。
螯合剂
通常放射性核素与配体的结合需要借助螯合剂。根据核素的不同,需要选择不同的螯合剂,常见的螯合剂包括DOTA、DTPA、NOTA、TETA等。
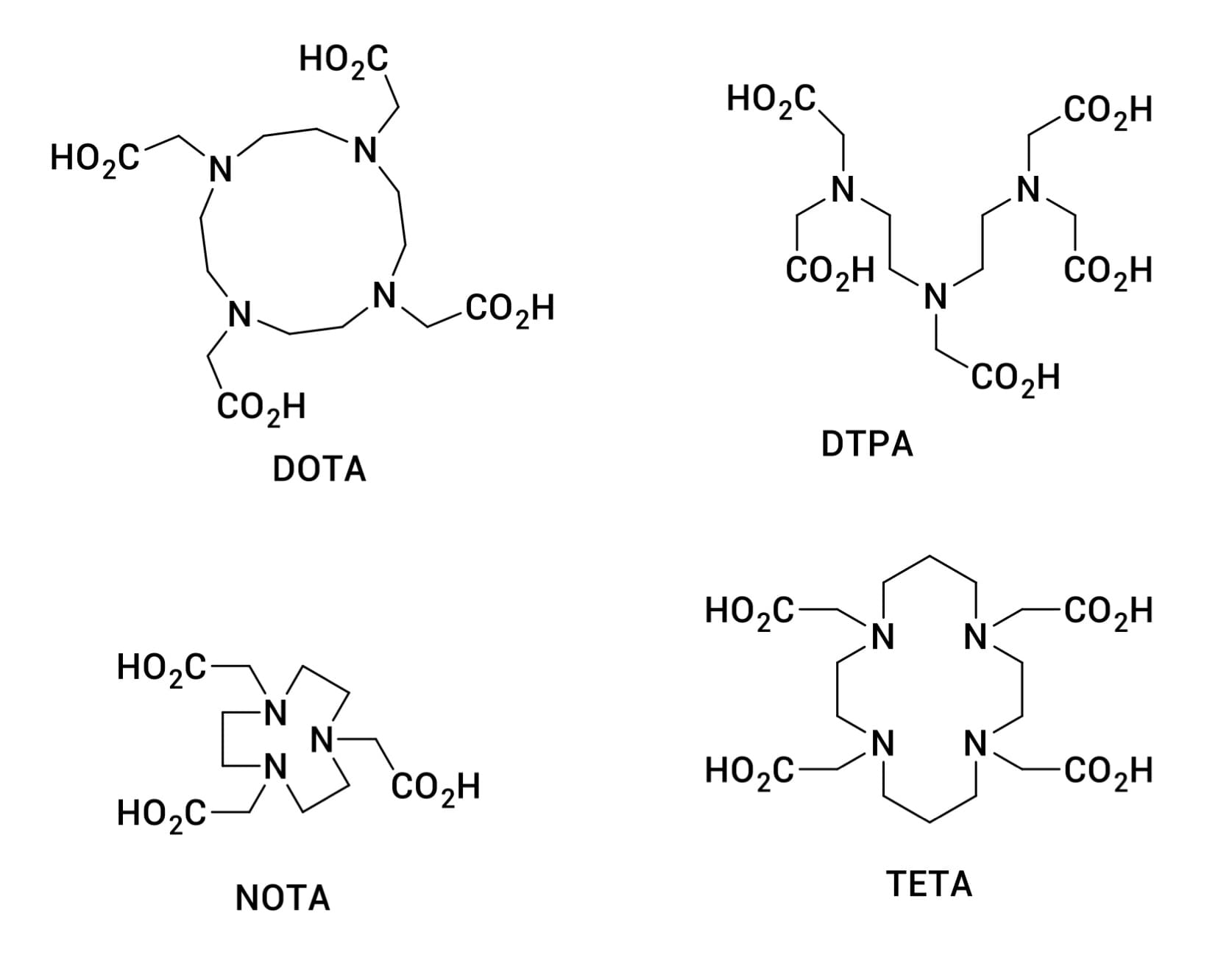
图2. 常见螯合剂的结构示意图
多肽偶联放射性核素药物(PRC)的作用原理和优势
PRC药物的作用原理
精准靶向与诊疗一体化是PRC药物的核心优势,其通过靶向多肽将放射性核素递送到目标病变部位,利用放射性核素发射的射线或粒子诱导细胞死亡。除直接杀伤靶细胞外,PRC还可借助辐射产生的“交叉火力”与“旁观者”效应,对邻近肿瘤细胞产生间接杀伤,甚至通过激活辐射诱导的免疫反应及远隔效应,实现对远处细胞的抑制。此外,基于同一靶向多肽搭载不同核素的策略,可在临床中实现“先诊断后治疗”的精准诊疗一体化流程[1]。
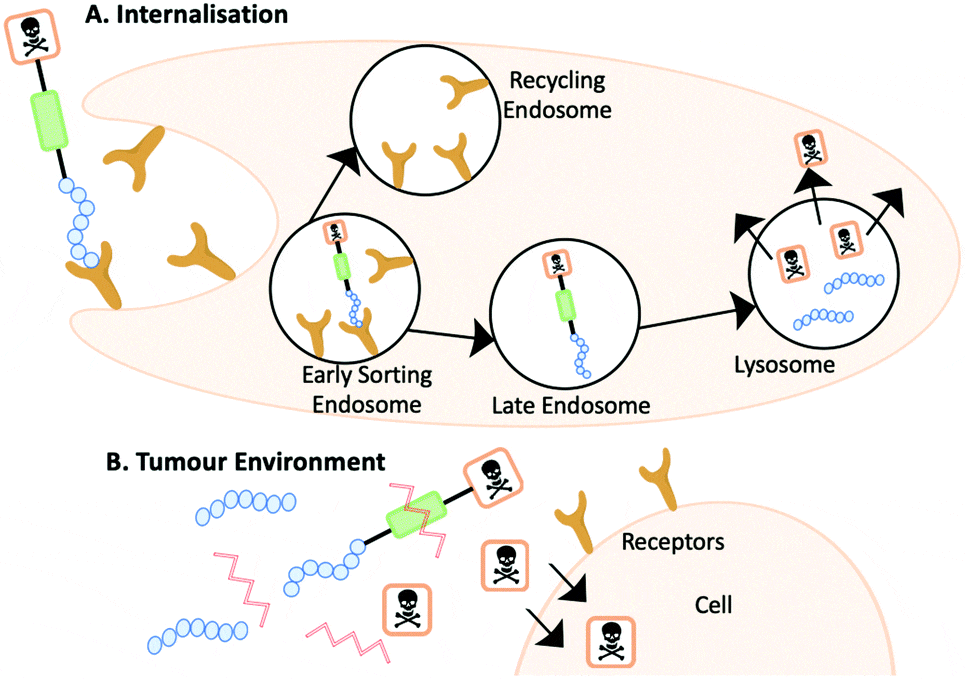
图3. PRC的作用机制示意图[2]
PRC药物的优势
PRC以靶点亲和力强、免疫原性低、组织穿透能力强、血液清除快等优势,在核素赛道中脱颖而出。
靶点亲和力高
鉴于PRC药物在进入血液循环后即释放辐射,其靶向特异性必须达到极高要求。Christoph Nitsche团队[3]对来自铋系列和砷系列的两种高亲和力肽(2b,3a)及其线性类似物(2,3)进行了系统比较。研究显示,多肽-铋双环化合物对链霉抗生物素蛋白的解离常数(KD)均在10 µM范围内,较其线性对应物降低了两个数量级,表明结构约束可显著增强PRC药物与靶点的亲和力,进而提升其药效。
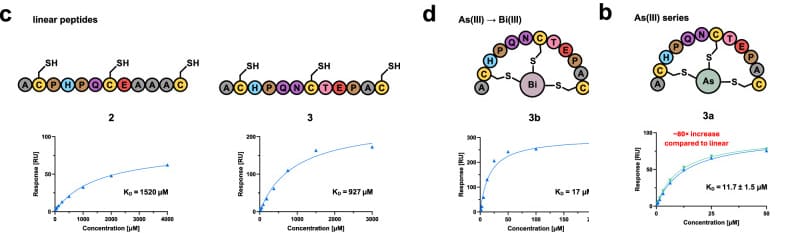
图4. 线性肽(2, 3)和肽-铋双环、肽-砷双环(2b, 3a)解离常数的比较[3]
双环肽分子具备与抗体类似的精准靶向特异性。以Bicycle®放射性偶联物(BRC)Pb-BCY20603为例,该分子能够以高亲和力结合肿瘤抗原MT1-MMP,并携带可释放α粒子的放射性核素铅-212。其临床前研究显示,Pb-BCY20603在注射24小时后,肿瘤部位的放射性摄取水平仍高于45%注射剂量(ID/g),并在啮齿类动物肿瘤异种移植模型中表现出良好的肿瘤靶向性和显著的抗肿瘤活性。
渗透能力强
抗体因分子量大、结构复杂,在肿瘤组织中易被血管屏障拦截,导致渗透效率降低。相比之下,多肽分子量较小,能够快速深入地渗透组织,从而实现从组织内部靶向病灶。PRC整合了多肽的优势,能够更快速地富集到肿瘤部位,实现对病灶的高效治疗。在结构方面,环肽展现出优于线性肽的胞质转运效率。以Pb-BCY20603为例,该药物采用双环肽技术,可穿透实体瘤中致密地结缔组织屏障,直达肿瘤核心区域,相较于传统生物制剂,具有显著的肿瘤穿透能力优势。
清除率高
多肽的特性使PRC药物具备可控的药物动力学半衰期和以肾脏为主的清除途径,从而避免了其他药物形式中常见的肝脏和胃肠道毒性。PRC药物优异的代谢性能,与肾脏代谢占主导地位高度相关,其在血液中能够被迅速清除,半衰期短有助于降低因脱靶辐射引起的毒副作用。例如,177Lu-DOTA-IBA在血液中清除速度较快,未与骨骼结合的部分主要通过泌尿系统排泄,注射4小时后血液中残留量仅为0.085 ± 0.011 % ID/g [4]。
多肽偶联放射性核素药物(PRC)的代谢特征和实验考量
PRC药物的代谢主要来源于放射性核素和多肽两个组成部分。在代谢过程中,核素存在脱落风险,可能对正常组织造成辐射毒性,因此除了关注核素多肽偶联物本身,也需要关注核素脱落后的多肽及其产物。多肽的化学和生物学性质决定了PRC药物在体内的生物学分布,PRC与靶点的亲和力和细胞摄取率与多肽的完整性高度相关,受体特异性c端氨基酸序列的酶切可能导致靶点亲和力和细胞摄取完全丧失,因此深入理解其代谢机制对多肽结构的优化与药物开发具有重要意义[5]。
PRC的代谢和清除特征
多肽的代谢机制多样,主要受其结构、相对分子质量、亲水性等因素影响,主要包括肽酶水解、内吞消除、靶点介导的消除和肾小球过滤等,其中以酶解消除和肾小球过滤为主。肾脏是其主要代谢器官,代谢产物主要通过尿液和粪便排泄[6]。
多肽主要通过肽酶水解代谢,肽酶分为外肽酶和内肽酶,广泛分布于肝、肾和胃肠道。内肽酶将多肽水解为寡肽,外肽酶再进一步水解为氨基酸。尽管多肽药物的代谢途径相对单一(主要是水解),但由于水解酶分布广泛,因此其代谢体系非常复杂,其中肝和肾的S9或匀浆是最常用的体系。(多肽药物的体外代谢体系详细介绍可参考:多肽药物的体外代谢研究:不同测试体系的比较与应用。)
多肽的分子构型直接影响PRC药物的稳定性,Christoph Nitsche团队[7]研究了线性肽、单环肽、双环肽和三环肽在蛋白酶靶标和人类血浆中的稳定性,结果显示在蛋白酶靶标实验中,线性肽和单环肽易于裂解,而三环肽在24小时内保持超过95%的稳定性;在人类血浆中,双环和三环肽在90分钟内表现出增强的稳定性(>65%)。综上,环肽在蛋白酶靶标(图5C-D)和人血浆(图5)中均有较好的稳定性。
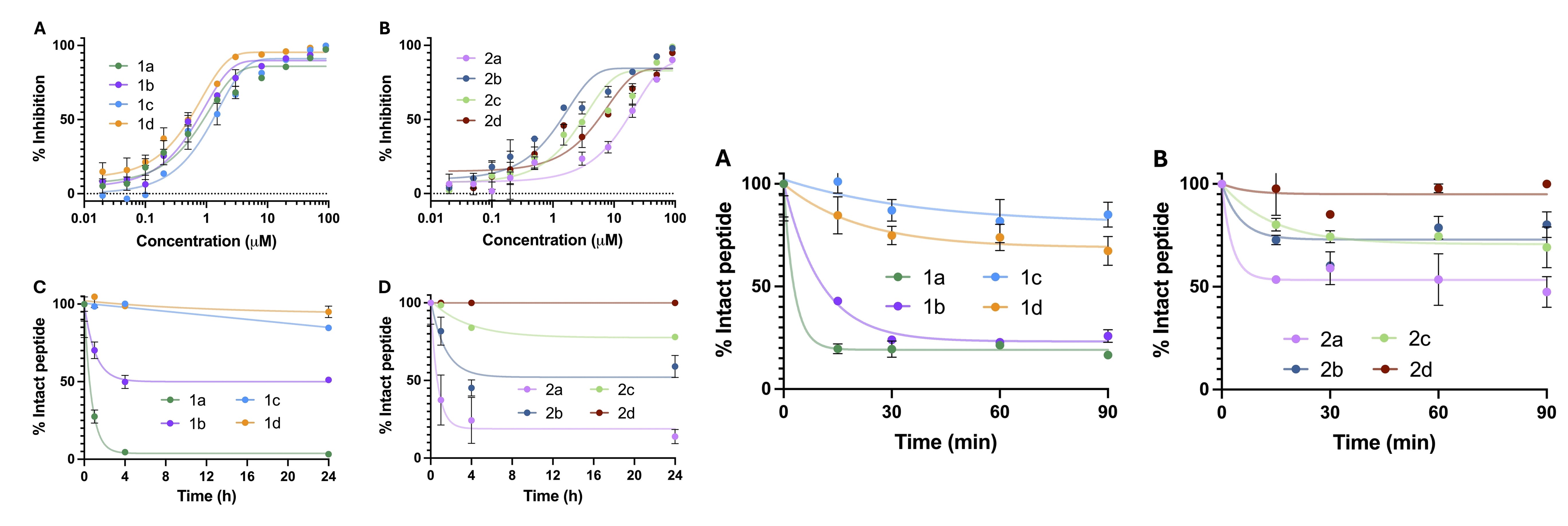
图5. 线性肽(1a, 2a)、单环肽(1b, 2b)、双环肽(1c, 2c)和三环肽(1d, 2d) 在蛋白酶靶标和人类血浆中的稳定性比较[7]
Voss Saan 等[10]研究了肽-铋双环在谷胱甘肽存在下的稳定性,研究表明在高达2 mM GSH存在下,48 h内未检测到化合物的水解。但在10 mM GSH的情况下,观察到30%的水解。另一研究[7]也表明(图6A-B),肽-铋双环2c表现出稍低的稳定性(>85%保持不变);但肽-铋三环(2d)在高达25当量浓度的GSH存在下保持>95%的完整性[7]。因此,不同浓度的GSH对多肽的稳定性影响不同,同时,相同GSH浓度对不同结构多肽(核素与巯基通过共价键结合的多肽)的影响也不同。同时,该研究还发现EDTA的浓度也会显著影响多肽的稳定性,在螯合剂EDTA存在的情况下,铋易与EDTA进行结合(图6C-D);无论是双环肽还是三环肽,在5~25个当量EDTA下,PRC剩余率均低于80%;相比于双环肽,肽-铋三环表现出更高的稳定性;但EDTA对不同序列多肽核素偶联物稳定性的影响也不同。
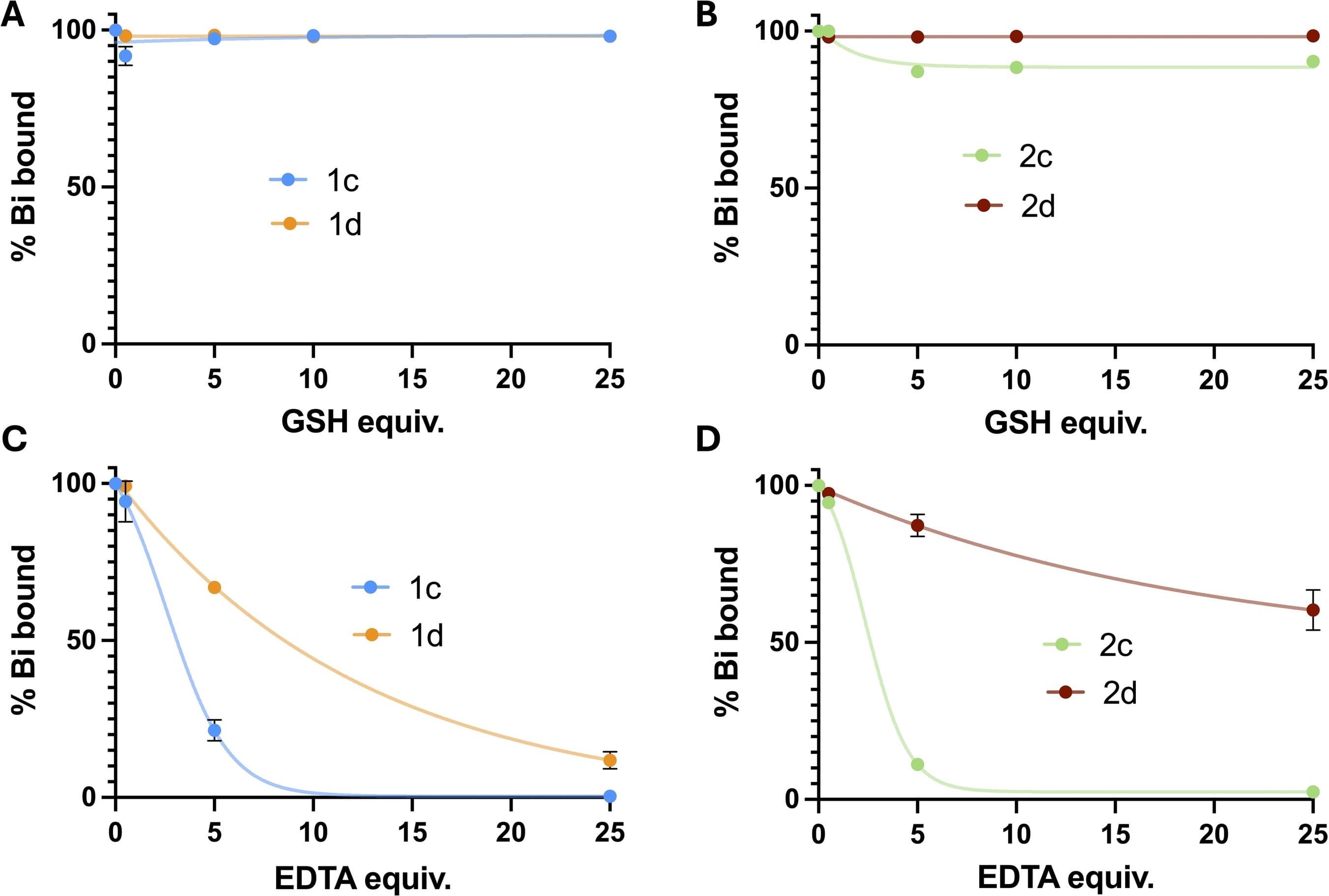
图6. 双环肽(1c, 2c)和三环肽(1d, 2d) 在GSH和EDTA中的稳定性[7]
Anton 等[8]开展了[177Lu]标记的MG类似物(DOTA-DGlu-Pro-Tyr-Gly-Trp-(N-Me)Nle-Asp-1Nal-NH2)的人体外和小鼠体内代谢研究,结果显示:MG类似物在人体外基质中的稳定性顺序为血清>肝匀浆>肾匀浆;同时还研究了它的4个主要代谢产物([177Lu]Lu-M1-[177Lu]Lu-M4)在血清中孵育24 h后的稳定性,比较发现当PRC或代谢产物与蛋白结合较低时,稳定性显著降低,因为高水平的游离放射性肽更容易被蛋白酶水解。小鼠体内研究结果显示,在注射药物60分钟后,全血中PRC剩余率为56.9%,同时检测到4个放射代谢产物([177Lu]Lu-M1-[177Lu]Lu-M3和[177Lu]Lu-M5),这4个放射性代谢产物的总占比为43.1%。给药60 min后的肝脏中,PRC剩余率为47.7%,同时还检测到6个放射代谢产物:[177Lu]Lu-M1-[177Lu]Lu-M6,总占比为82.0%。在给药后的肾脏和尿液中,也观察到了相同的代谢产物(除M7),其中放射性代谢产物[177Lu]Lu-M1、[177Lu]Lu-M3和[177Lu]Lu-M7占比较低(<10%);其它4个放射代谢产物占比均超过10%,且有增加趋势;而标记的MG类似物在肾脏和尿液中仅占7.0%和18%。
综上,标记的MG类似物在全血和肝脏中均表现出较好的稳定性,而在肾脏中稳定性较差,因此肾脏被认为是其主要的清除途径。肝和肾脏中检测到的7个代谢产物由C末端酰胺键水解及其C端肽键依次水解而形成,但未观察到谷氨酸(D-Glu)和脯氨酸(L-Pro)之间肽键的水解,说明引入到肽骨架中的三级酰胺键可能起到了稳定作用。表3汇总了小鼠体内不同放射性代谢产物的占比。
表3. 不同基质中放射性代谢产物的占比[8]
Peptide | Blood | Liver | Kidney | Urine | ||||
30 min | 60 min | 30 min | 60 min | 30 min | 60 min | 30 min | 60 min | |
[177Lu]Lu-1 | 64.1% | 56.9% | 53.9% | 47.7% | 18.0% | 7.0% | 19.4% | 18.0% |
[177Lu]Lu-M1 | 9.9% | 5.8% | 4.8% | 4.6% | 2.5% | - | 1.4% | - |
[177Lu]Lu-M2 | 3.8% | 7.3% | 7.2% | 6.9% | 20.7% | 12.3% | 40.5% | 40.3% |
[177Lu]Lu-M3 | 17.0% | 20.4% | 8.5% | 5.6% | 7.9% | - | 9.5% | 9.8% |
[177Lu]Lu-M4 | - | - | 2.9% | 2.6% | - | - | - | - |
[177Lu]Lu-M5 | 5.3% | 9.6% | 14.4% | 12.9% | 27.3% | 23.7% | 28.7% | 31.3% |
[177Lu]Lu-M6 | - | - | 8.3% | 19.7% | 23.6% | 53.2% | - | - |
[177Lu]Lu-M7 |
| - | - | - | - | 3.8% | - | - |
[177Lu]Lu-M8 | - | - | - | - | - | - | - | - |
PRC药物的体外代谢研究考量
鉴于放射性同位素实验开展门槛极高,若所选放射性核素已有临床使用经验,PRC药物在临床前研究可采用非放射性的核素偶联药物进行实验[9]。
在PRC药物的代谢研究中,实验体系的设计需综合考虑多种因素,以确保对药物代谢行为的准确评估。与多肽药物的代谢相比,除了要考虑肽酶水解,还要关注连接子和螯合剂的断裂。由于核素不需要与细胞直接接触就可发挥辐射效果,因此在研究PRC药物的代谢时还需关注核素是否脱落,进而评估核素脱落造成的毒性风险。放射性核素通常通过螯合剂与多肽连接,当体内存在更强螯合剂时,金属核素可能会被更强的螯合剂捕获而降低药效。其中,谷胱甘肽(GSH)和乙二胺四乙酸(EDTA)是两个重要的考量因素。
血浆的易获取性和丰富的肽水解酶使其成为体内外药物代谢研究的首选基质。在血浆样本制备过程中,为防止血液凝固需要添加抗凝剂,常用种类包括EDTA和肝素钠,EDTA可能影响血浆中某些酶活或PRC的核素稳定性,进而导致实验结果的偏差。因此在设计实验方案时,应充分考虑抗凝剂的种类及其对实验结果的潜在影响,建议优先使用肝素钠作为抗凝剂,以确保数据的可靠性和可重复性。
当PRC药物中放射性核素与多肽的硫原子结合时,需进一步评估体系中GSH浓度对药物代谢的影响。研究表明,含巯基化合物的竞争可能影响三种肽硫醇与铋的结合。为了更好地评估PRC药物在体内的稳定性,含GSH的孵育体系(如肝S9、匀浆或肝细胞)可能更适合研究PRC药物的代谢稳定性。
结语
随着人口老龄化进程加速和全球癌症发病率的持续增加,制药企业积极布局核药领域,推动放射性药物市场进入快速发展阶段。多肽偶联放射性核素药物(PRC)作为新兴的肿瘤精准诊疗药物,凭借其高靶点亲和力、低免疫原性、良好组织穿透性、快速血液清除等优势,已成为核药研发的重要方向之一。
然而,PRC在体内代谢过程中仍面临多肽易水解与核素脱落等风险,可能对非靶器官造成辐射损伤。因此,开展系统的代谢产物鉴定研究可以全面表征多肽水解和核素脱落的情况,进而为PRC的体内外药效和毒性研究提供参考。基于这一需求,药明康德DMPK建立了完整的PRC代谢产物鉴定研究平台,以UPLC-UV-HRMS技术为核心,结合多种专业数据处理软件,为PRC药物的代谢行为解析与优化提供可靠支持,助力肿瘤精准诊疗药物的高效研发。
作者:郭丙倩,李瑞兴,曹卫群
编辑:富罗娜·克里木,钱卉娟
设计:张莹莹
药明康德DMPK依托中国(上海、苏州、南京和南通)和美国(新泽西)的研发中心,提供从早期筛选、临床前开发、到临床研究阶段的综合型药代动力学服务,助力您快速推进药物研发流程。拥有上千人的研发团队,服务超1600家全球客户,具有超过十五年的新药申报经验,已成功支持超过1700个新药临床研究申请(IND)。
点击此处与我们的专家进行联系
参考
[1] 放射性体内治疗药物临床评价技术指导原则(2023)。
[2] Bethany M. Cooper, Jessica Iegre, Daniel H. O’ Donovan, et al. Peptides as a platform for targeted therapeutics for cancer: peptide–drug conjugates (PDCs). Chem. Soc. Rev, 2021, 50: 1480-1494. 10.1039/d0cs00556h.
[3] Sven Ullrich, Upamali Somathilake, Minghao Shang, et al. Phage-encoded bismuth bicycles enable instant access to targeted bioactive peptides. Communications Chemistry, 2024, 7: 143.
[4] Hongmei Li, Wenjie Pei, Xiqun Yang, et al. Biodistribution and dosimetry of 177Lu-DOTA-IBA for therapy of bone metastases. EJNMMI Research, 2024, 14: 30.
[5] 放射性体内诊断药物临床评价技术指导原则(2020)。
[6] 姚金凤。多肽类药物代谢研究进展[J].中国药理学通报,2013, 29(7):5. doi:10.3969/J.issn.1001-1978.2013.07.003.
[7] Lani J. Davies, Pritha Ghosh, Sauhta Siryer, et al. Peptide–Bismuth Tricycles: Maximizing Stability by Constraint. Chem. Eur. J, 2025, 31: e202500064.
[8] Anton Amadeus Hörmann, Maximilian Klingler, Maliheh Rezaeianpour, et al. Initial In Vitro and In Vivo Evaluation of a Novel CCK2R Targeting Peptide Analog Labeled with Lutetium-177. Molecules, 2020, 25, 4585. doi:10.3390/molecules25194585.
[9] 放射性体内诊断药物非临床评价技术指导原则(2021)。
[10] Voss Saan, Adair Liam D, Achazi Katharina, et al. Cell-Penetrating Peptide-Bismuth Bicycles. Angew. Chem. Int. Ed, 2024, 63, e202318615.
加入订阅
获取药物代谢与药代动力学最新专业内容和信息