抗体-寡核苷酸偶联物(antibody-oligonucleotide conjugates, AOC)是由抗体与寡核苷酸通过特定技术偶联而成的生物药。它借助抗体的靶向递送能力与寡核苷酸的靶点特异性,将治疗性寡核苷酸递送至特定细胞或组织,可有效解决寡核苷酸药物在肝外组织中的递送挑战,为遗传疾病、肿瘤等难治性疾病提供了新的治疗思路[1]。AOC研究与临床开发进展迅速,代表性企业如Avidity Biosciences其候选药AOC 1001在2023年10月公布的临床数据(NCT05027269)显示,患者肌肉中致病蛋白DMPK(dystrophia myotonica protein kinase,强直性肌营养不良蛋白激酶)水平平均下降约45%;该候选药于2024年第二季度成为全球首个进入临床III期的AOC药物。此外,Dyne Therapeutics、Tallac Therapeutics、Denali等公司也持续推进各自的AOC研发管线,覆盖肌肉疾病、中枢神经系统疾病及肿瘤等多个领域(表1)。
与小分子或单一生物大分子不同,AOC为“抗体+寡核苷酸+连接子”的三元复合体,每一部分的理化特性及其相互作用都会显著影响其药效及ADME特征。因此,深入了解AOC的结构特征及其对ADME的影响具有重要价值:一方面可为体内外代谢产物鉴定实验、PK实验设计与暴露‑反应关联的建立提供依据;另一方面,可指导分子设计与偶联策略优化,如选择稳定或可裂解连接子、优化偶联位点与OAR(oligonucleotide‑to‑antibody ratio,寡核苷酸抗体比)、改进寡核苷酸修饰,从而平衡体内稳定性、靶向递送与细胞内释放以提高疗效并降低脱靶毒性,为安全性评价与临床转化提供支撑。
为此,我们将发布系列文章,系统总结AOC药物的结构特征(抗体类型、寡核苷酸种类与化学修饰、偶联位点与化学连接子以及OAR等)与功能的关系,并综述AOC的药代动力最新研究进展,为相关研究提供参考。
表1. 部分公司在研AOC药物信息汇总[2]
药物名称 | 公司 | 抗体类型 | 药物载荷 | 作用靶点 | 作用组织 | 适应症 | 研究阶段 | 最新临床结果 |
AOC 1001 | Avidity | 靶向TfR1的单抗 | DMPK siRNA | DMPK | 肌肉组织 | DM1 | III期临床 | 接受治疗的参与者中,DMPK平均降低了45% |
AOC 1044 | Avidity | 靶向TfR1的单抗 | Exon-44-skipping PMO | Exon-44 | 肌肉组织 | DMD | III期临床 | 抗肌肉萎缩蛋白(dystrophin) 显著增加 |
AOC 1020 | Avidity | 靶向TfR1的单抗 | DUX 4 siRNA | DUX 4 | 肌肉组织 | FHSD | III期临床 | cDUX生物 标志物下降 |
DYNE-101 | Dyne | 靶向TfR1的抗原结合片段 | DMPK ASO | DMPK | 肌肉组织 | DM1 | I/II期临床 | 患者肌强直 症状改善 |
DYNE-251 | Dyne | 靶向TfR1的抗原结合片段 | Exon-51-skipping PMO | Exon-51 | 肌肉组织 | DMD | I/II期临床 | 患者平均抗肌肉萎缩蛋白(dystrophin) 水平提升 |
DYNE-302 | Dyne | 靶向TfR1的抗原结合片段 | DUX4 ASO | DUX4 | 肌肉组织 | FSHD | 临床前 | 无 |
未披露 | Denali[3] | 借由Fc区域功能化靶向TfR1的单抗 | 未披露的ASO | 未披露 | 脑 | 未披露 | 临床前 | 无 |
未披露 | Ionis | 靶向CD29的单抗 | 未披露的siRNA | 未披露 | 未披露 | 未披露 | 临床前 | 无 |
Tac-001 | Tallac | 靶向CD22的单抗 | CpG (TLR9激动剂) | TLR9 | B细胞 | 晚期实 体瘤 | I/II期临床 | 部分患者 疾病稳定(stable disease,SD) |
ALTA-002 | Tallac | 靶向SIRPα的单抗 | CpG (TLR9激动剂) | TLR9 | 树突状细胞 | 实体瘤 | 临床前 | 无 |
注:TfR1:transferrin receptor 1(转铁蛋白受体1);CD29:整合素β1 (integrin beta-1);CD22:Siglec-2(唾液酸结合Ig样凝集素2);DMPK:dystrophia myotonica protein kinase(强直性肌营养不良蛋白激酶);siRNA:small interfering RNA(小干扰RNA);PMO:phosphorodiamidate morpholino oligomer(磷酸二酰胺吗啉低聚物);DUX4:double homeobox protein 4(双同源盒蛋白4);ASO:antisense oligonucleotide(反义寡核苷酸);CpG:cytosine phosphoric acid guanine(胞嘧啶磷酸鸟嘌呤);TLR9:toll like receptor(Toll样受体9);DM1:myotonic dystrophy type 1(强直性肌营养不良1型);DMD:duchenne muscular dystrophy(杜氏肌营养不良症);FSHD:facioscapulohumeral muscular dystrophy(面肩肱型肌营养不良症)。
AOC药物的结构特征
AOC药物主要由抗体、连接子和寡核苷酸三部分通过不同的偶联方式组合而成,各组分结构的协同作用决定了药物的靶向效率、载荷释放动力学及最终疗效。其作用机制主要包括:
靶向识别:抗体部分特异性识别并结合靶细胞表面抗原;
内化与转运:抗原-抗体复合物经内吞作用进入细胞,形成内吞体,内吞体在细胞内与溶酶体结合;
载荷释放:可裂解连接子在自身裂解后释放出载荷;不可裂解连接子作为有效载荷的一部分,通过抗体骨架的降解实现释放。释放出的活性寡核苷酸(游离或复合物形式)需进一步从溶酶体逃逸至胞质并抵达其作用位点;
基因调控:siRNA通过加载至RNA诱导沉默复合体(RNA-induced silencing complex,RISC),经由AGO2蛋白切割靶mRNA实现基因沉默;ASO则通过与mRNA互补配对形成杂合体后的空间位阻阻止mRNA翻译、与pre-mRNA结合调控可变剪接(如诱导外显子跳跃或促进外显子包含)或招募RNase H降解靶RNA等方面实现基因调控。
综上所述,从靶向递送、内化转运到溶酶体作用的载荷释放,寡核苷酸的溶酶体逃逸与细胞内的基因调控,构成了一个精密调控网络,三个部分在其中都起到了至关重要的作用。本文将重点探讨AOC的抗体与寡核苷酸的结构与功能的关系;在后续文章中,将进一步综述偶联位点与连接子的结构特征及其功能影响,并汇总AOC的药代动力学研究最新进展。
抗体载体
抗体主要承担靶向递送功能,常见的抗体形式包括单克隆抗体(monoclonal antibodies, mAbs)、多克隆抗体(polyclonal antibodies, pAbs)、重组抗体(recombinant antibodies)、纳米抗体(nanobodies)、双特异性抗体(bispecific antibodies, BsAbs)和抗体片段(antibody fragments)等,其中mAbs为AOC中最常用的抗体类型,常用免疫球蛋白G(IgG)为基本骨架,均一性好。对于mAbs,不同作用位点的抗体整体、抗原结合片段(fragment antigen-binding,Fab)或可结晶片段(fragment crystallizable,Fc)的定点改造与偶联策略被不同公司广泛采用,下文将从抗体结构、抗体选择与设计两方面展开讨论。
抗体结构
IgG骨架的抗体是由两条相同的重链和两条相同的轻链组成的“Y形”结构,“Y”的两个臂为Fab区,包含由重链和轻链各三个互补决定区(CDRs)构成的抗原结合位点,负责特异性识别抗原表位。“Y”的主干称为Fc区,属于恒定区,决定抗体亚型并介导Fc受体结合、补体活化及FcRn介导的回收延长半衰期等效应[4]。具体结构和功能位点如图1所示。
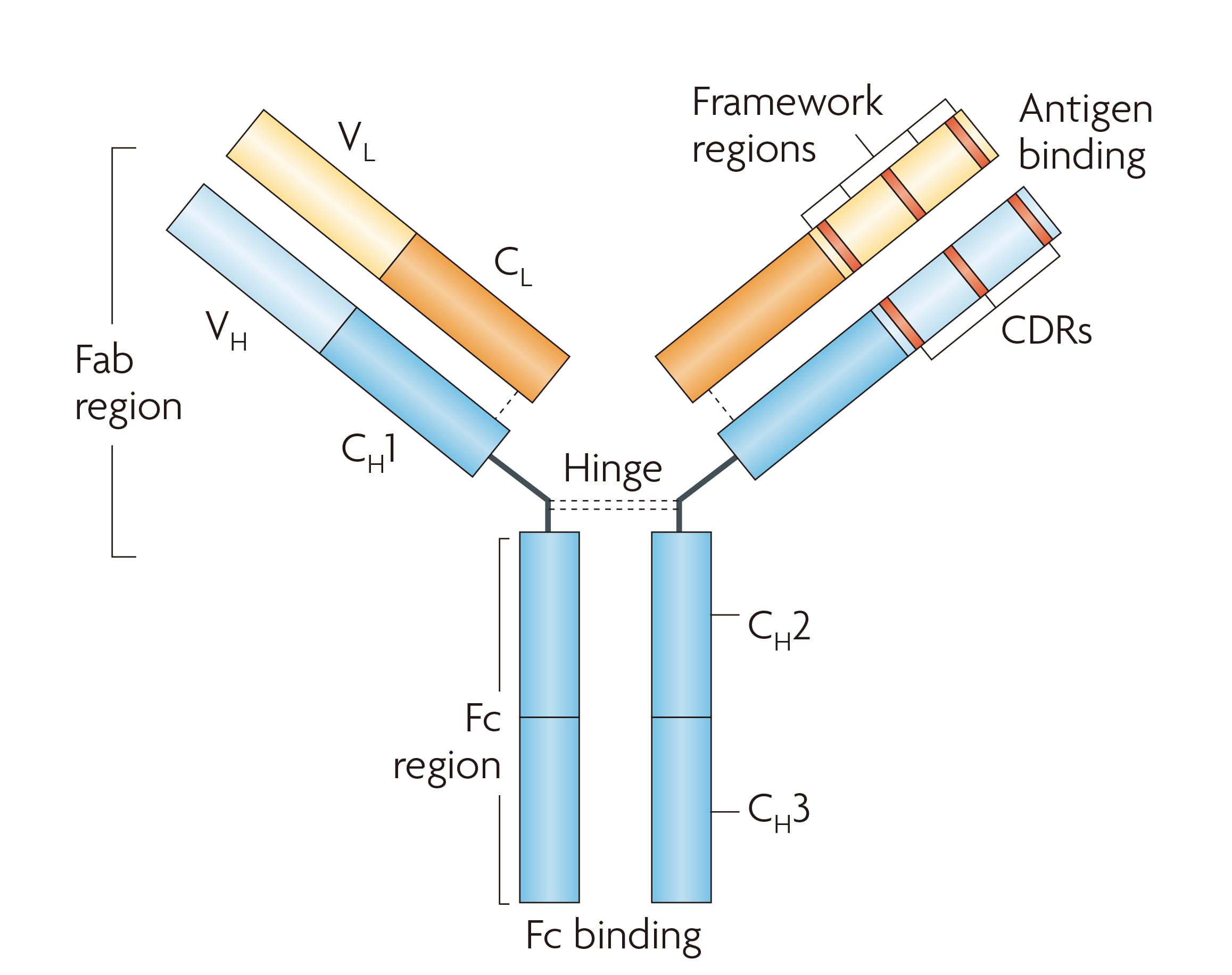
图1. 抗体的结构[5]
抗体选择与设计
针对不同靶点,目前在研的AOC所用抗体多样,包括anti-TfR1、anti-CD29、anti-CD22、anti-SIRPα、anti-EGFR[6]等。这些抗体的选择与设计主要基于一定的综合考量,如目标组织细胞表面的对应受体/抗原表达水平与可结合性、结合后能否诱导内吞、非目标组织中的分布、可用于位点专一偶联的残基类型,以及是否需要保留或削弱Fc功能以影响半衰期与免疫效应等。
如表1与图2所示,针对肌肉靶向的anti‑TfR1,Avidity采用全长单克隆IgG骨架,借助Fc–FcRn回收显著延长血浆半衰期,可实现持续暴露与延长给药时间;而Dyne则采用Fab片段,体积小、组织渗透性更好、且无Fc介导效应,有助于药物更容易渗透到肌肉组织并到达靶点,同时降低免疫相关风险,但半衰期较短、可能需更频繁给药或额外修饰。 两者权衡的核心在于在提高组织穿透性与维持系统性暴露时长之间取得平衡,同时考虑是否保留或去除Fc介导的功能(如FcRn回收以延长半衰期、以及FcγR-介导的抗体依赖性细胞毒性和补体依赖性细胞毒性。)及由此带来的免疫安全性影响。与Avidity及Dyne不同,Denali的anti‑TfR1针对中枢神经系统(CNS)方向,通过工程化抗体Fc结构域,增强与血脑屏障上TfR的相互作用,借助受体介导的内吞与跨胞转运将抗体及寡核苷酸载荷输送入脑,为中枢神经系统疾病治疗提供了可行路径[7]。
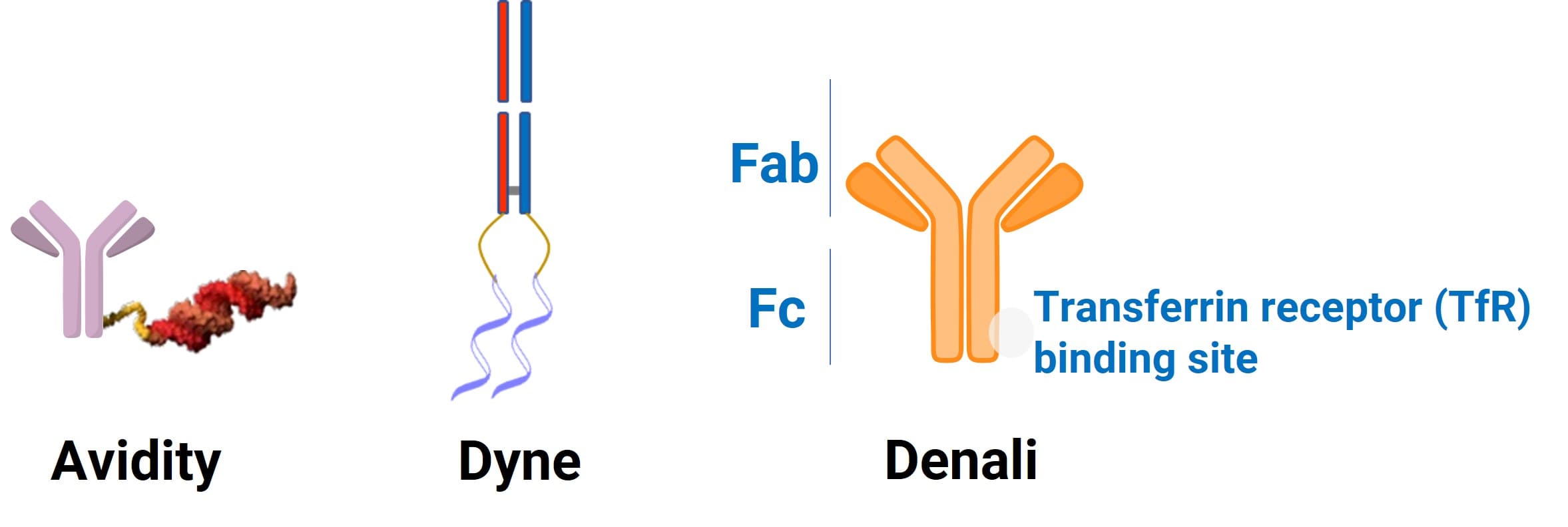
图2. 三家公司的抗体设计比较
此外,在Ionis公开的专利中[8],以anti‑CD29的全长或Fab两种形式制备了AOC。其中全长IgG的Fc区域通常有两条N-型糖链(N-glycan),采用N-glycan位点偶联会得到OAR=1与OAR=2的混合物(同时可能存在未偶联的物质,其OAR=0)。该专利以此方法制备得到混合OAR的AOC,其OAR1和OAR2比例约为1:1,而对Fab则采取一定的策略,获得OAR为1的AOC,如图3所示。研究表明[9],抗体上连接的寡核苷酸数量会显著影响AOC的体内动力学与疗效:高OAR可能增加分子异质性、改变亲水/疏水性和Fc功能暴露,从而加速清除并降低有效暴露与疗效。因此,在优化AOC时需综合权衡OAR、偶联位点、连接子结构及稳定性等因素与体内分布及清除特性之间的相互关系,相关研究进展我们将在下一篇文章中详细介绍。
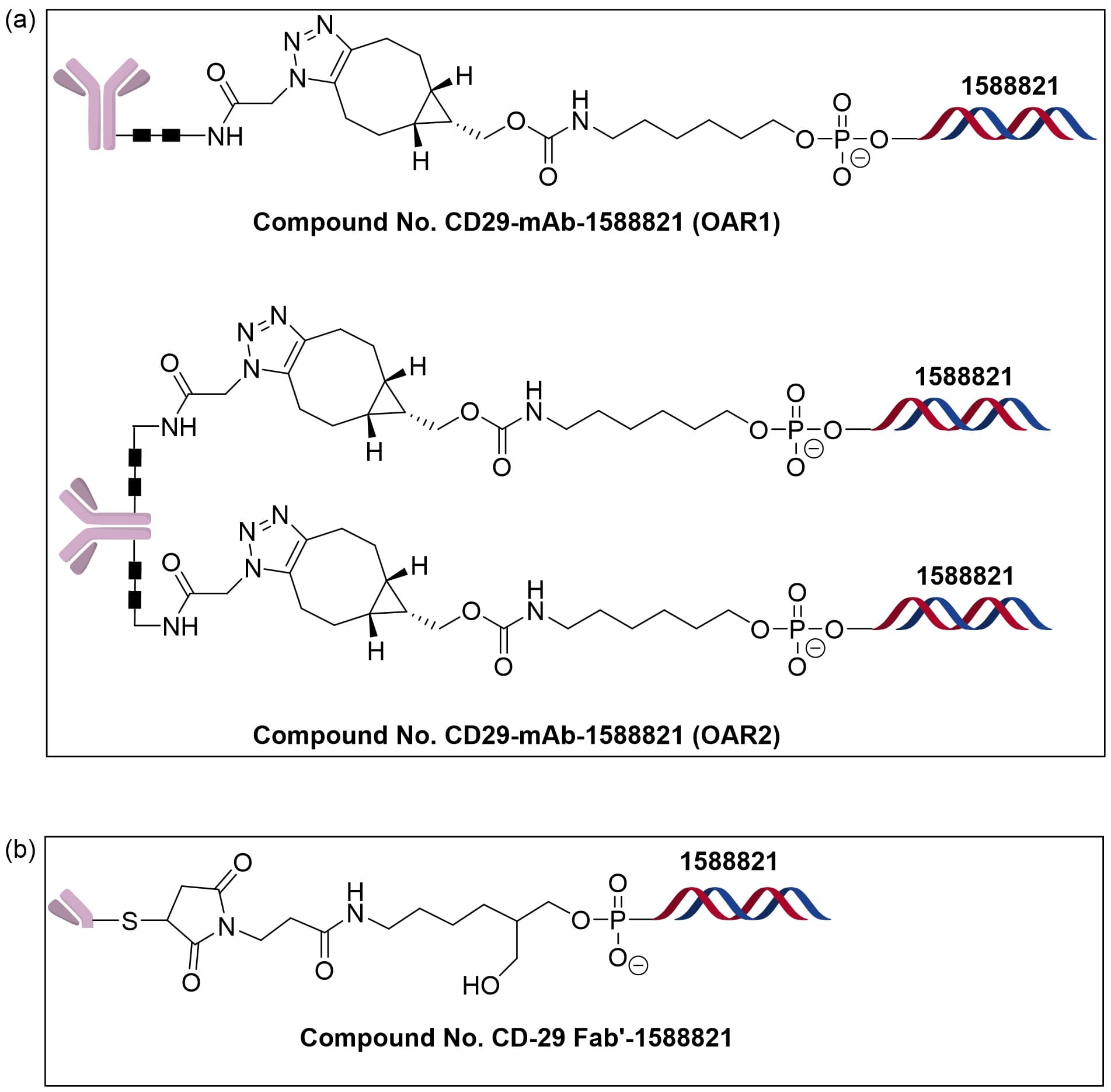
图3. 以anti-CD29的不同形式制备的AOC:全长抗体(a)和Fab(b)
综上,抗体在AOC中承担核心的靶向与递送功能,但不同靶点、抗体骨架/构型与工程化改造,以及偶联工艺会显著影响AOC的药代学特性(半衰期、组织分布、内化途径等)与免疫安全性。成功的AOC设计需在靶向性、受体介导内化后内体-溶酶体内的载荷释放与溶酶体逃逸效率、整体ADME行为与安全性之间进行系统性权衡;常用的协同优化策略包括受体选择与亲和力调控、抗体骨架工程(如去/保留Fc功能、糖基化调整)、位点特异性偶联及连接子(linker)的化学设计,以实现最佳疗效与安全性平衡。
寡核苷酸载荷
如表1所示,在研AOC药物中,常用的寡核苷酸类型主要为siRNA和ASO。siRNA为长度约20–25个核苷酸的双链RNA,ASO则为长度约15–25个核苷酸的单链RNA;二者均由碱基、糖(核糖或脱氧核糖)和磷酸骨架构成,未经修饰的ASO和siRNA在生物体内环境中稳定性均较差,但作用机制存在显著差异。下文将分别介绍常用的化学修饰以提高稳定性,并讨论在AOC设计中如何在siRNA与ASO之间进行选择。
寡核苷酸的化学修饰
寡核苷酸固有的负电荷、高极性、较大的分子量及对核酸酶的敏感性,使其在体内面临酶解、细胞膜通透性差与免疫识别等多重障碍,体内稳定性和靶向效率均受限,而化学修饰可极大增加其稳定性[10]。尽管偶联至抗体可为寡核苷酸提供一定保护。但Toshima[7]等的研究表明,其合成的AOC中siRNA片段在血浆和肿瘤组织中发生水解,进而可能削弱siRNA的内体逃逸和靶区富集。这表明即便在AOC中,寡核苷酸仍需通过化学修饰来提升稳定性,这些化学修饰的主要位点为磷酸骨架、糖环及碱基(图4),相关修饰及对应作用归纳如表2所示[10]。合理组合这些修饰策略,是优化AOC药物疗效的重要途径。
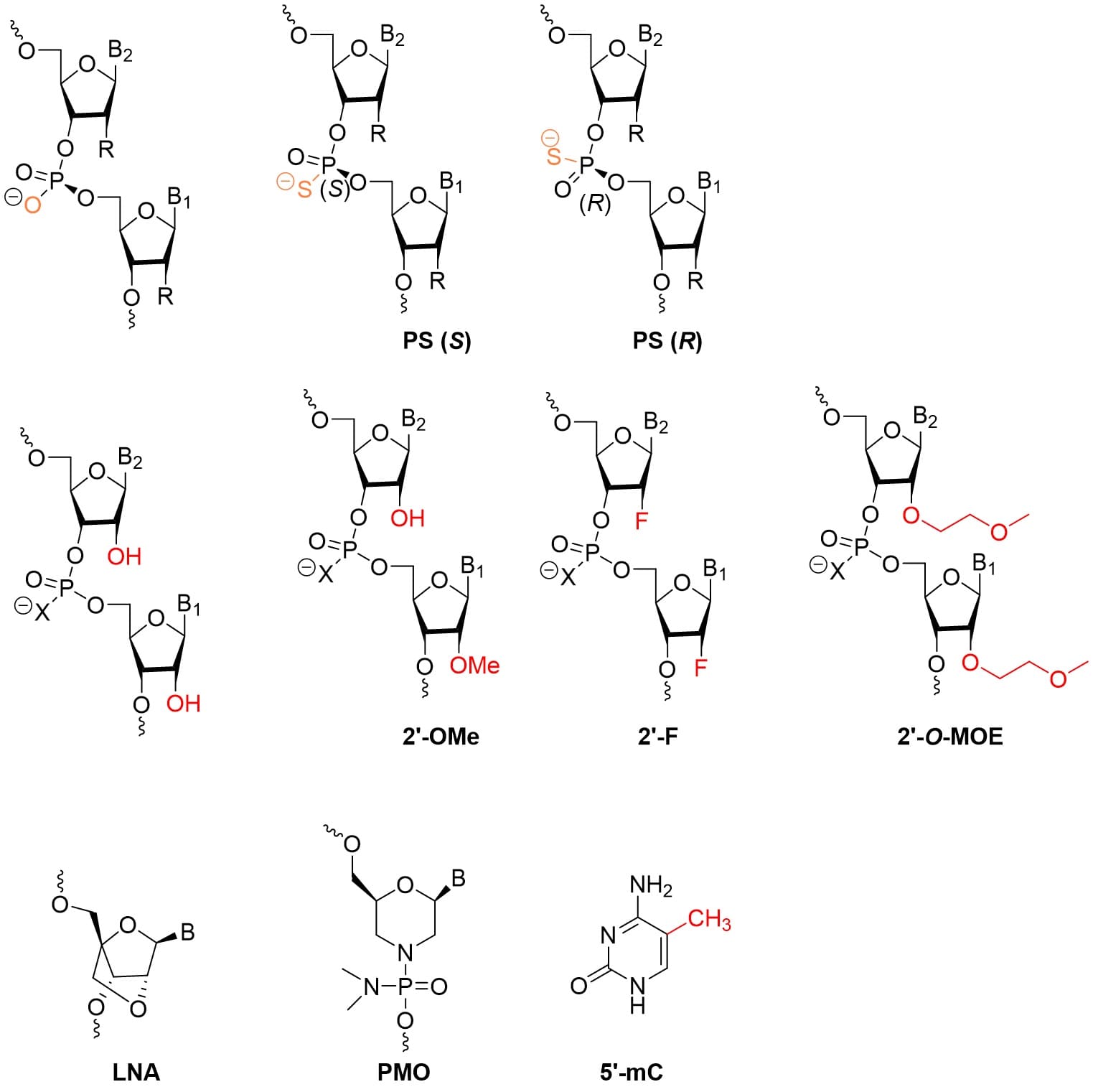
图4. 常见的寡核苷酸化学修饰策略
表2. 寡核苷酸的主要修饰类型及其作用
修饰位点 | 常见修饰 | 功能 |
糖环(2'-位) | 2'-O-甲基(2'-OMe) | 增强核酸酶抗性,减少免疫刺激 |
2'-氟(2'-F) | 提高热稳定性(Tm值) | |
锁核酸(LNA) | 提高杂交亲和力和稳定性 | |
磷酸骨架 | 硫代磷酸酯(PS) | 抗核酸酶降解,增强蛋白结合 |
磷酰二胺吗啉代(PMO) | 电荷中性,减少非特异性相互作用 | |
碱基 | 5-甲基胞嘧啶(5-mC) | 提高C-G配对稳定性,可降低免疫识别 |
寡核苷酸的选择
在当前AOC药物研发中,针对同一靶标可以采用不同类型的寡核苷酸。例如,Avidity的AOC 1001采用siRNA,而Dyne的Dyne‑101采用ASO。二者均靶向突变的DMPK基因,以消除CUG重复形成的发卡结构、恢复MBNL(肌盲样蛋白)功能,从而治疗I型强直性肌营养不良(DM1)。两者的主要差异为:
AOC 1001(siRNA)
siRNA为亲水、带负电的双链RNA,向细胞核渗透能力相对有限,通常更易在细胞质分布,并借助含AGO2的RISC复合体实现对靶mRNA切割。Avidity在公开资料中侧重于DMPK基因下调这一结果,未在相关材料中明确限定亚细胞作用位点。
Dyne-101(ASO)
ASO为单链RNA,能进入细胞核,且通常表现出相对疏水的性质。Dyne的策略是基于突变的DMPK mRNA滞留于细胞核的观点,而ASO可进入细胞核直接与靶mRNA结合并招募RNase H实现降解。
两家公司在寡核苷酸类型上的选择反映了不同的AOC药物设计策略,但最终疗效仍需以临床和转化研究数据为准。在选择siRNA还是ASO时,应综合考量理化性质、细胞/亚细胞分布、效力、内体逃逸与安全性等多方面因素。图5可用于直观比较两类寡核苷酸在细胞内的典型分布与作用机制。
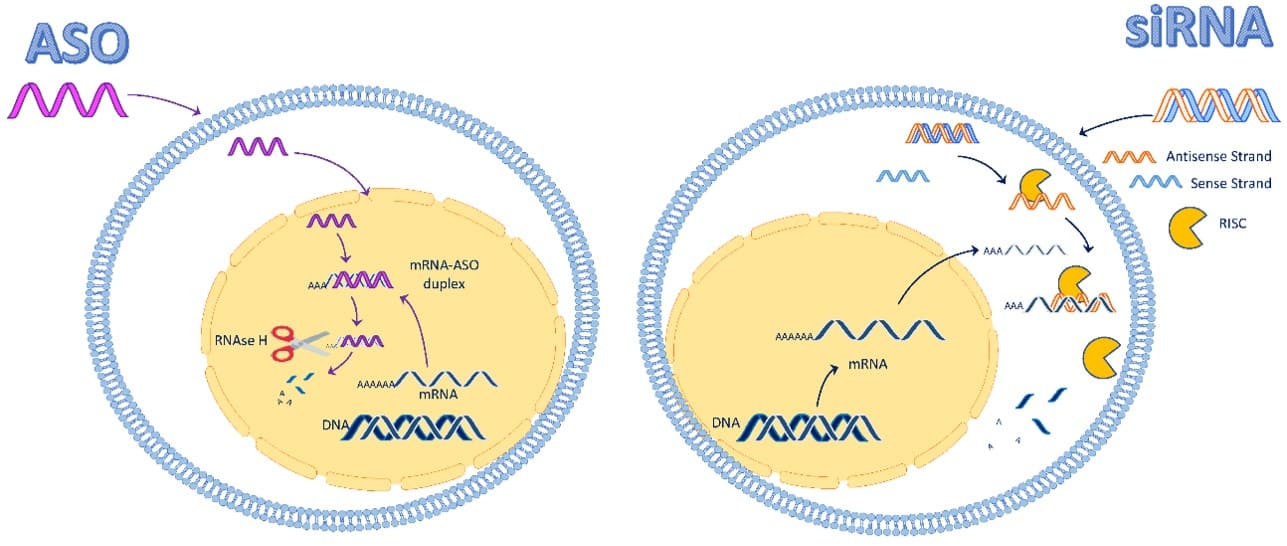
图5. siRNA与ASO在细胞中的分布及作用机制[11]
结语
本文综述了在研AOC药物的研发进展,重点讨论了其抗体与寡核苷酸部分的结构-功能关系。抗体结构、偶联位点与偶联方式(连接子与OAR)共同影响循环半衰期、组织分布与受体介导的内吞等行为。寡核苷酸通常在体内稳定性相对较差,其体内命运主要受磷酸骨架与糖环或碱基修饰、链型与长度、与蛋白的相互作用及与载体的偶联策略等因素影响;不同寡核苷酸的选择应结合其胞内分布特征与靶基因的致病机制加以权衡。
深入理解抗体与寡核苷酸各自的结构特性及其对ADME的影响,是AOC设计与临床转化的基础。将两类分子优势结合的AOC虽为跨组织递送提供了新机遇,但其复杂结构也带来了更为复杂的代谢途径与分析挑战——复杂的分子构型增加了代谢研究难度,充分的结构表征不仅为开展ADME研究提供基础,也为合理设计与解读PK实验提供必要依据。值得注意的是,连接子既是抗体与寡核苷酸之间的化学桥梁,其化学结构、偶联位点与释放机制又会深刻影响AOC的稳定性、靶组织释药效率及体内代谢命运。下一篇我们将着重探讨AOC连接子的结构特征与偶联方式,以及其对于AOC的药效、ADME和PK特征的影响,以期完整阐明AOC的结构-功能关系,并为相关研究提供参考。
药明康德DMPK基于对AOC药物结构特征及其ADME/PK性质的理解 ,已建立整合性DMPK研究平台,可支持开发者在不同阶段更加高效、准确地评估AOC药物的体内外ADME特征,深入解析其药效与安全性之间的关联,为后续的安全性评价和临床转化研究提供坚实的支撑。
作者:覃勇,施立琦,张洪,曹卫群
编辑:富罗娜·克里木,钱卉娟
设计:张莹莹
药明康德DMPK依托中国(上海、苏州、南京和南通)和美国(新泽西)的研发中心,提供从早期筛选、临床前开发、到临床研究阶段的综合型药代动力学服务,助力您快速推进药物研发流程。拥有上千人的研发团队,服务超1600家全球客户,具有超过十五年的新药申报经验,已成功支持超过1700个新药临床研究申请(IND)。
点击此处与我们的专家进行联系
参考
[1] Z. Xiaoxia, L. Dongke, G. Linjie, L. Ji, C. Hongxu, and G. Lihai, “Application of Capillary Zone Electrophoresis (CZE) and High resolution mass spectrometry (HRMS) in the components separation and structures confirmation of Antibody- oligonucleotide conjugates (AOC),” pp. 1–4, 2021.
[2] M. A. Jian, Y. U. Tonglin, C. U. I. Shuaishuai, H. E. Yujian, and W. U. Li, “R esearch Advances in Oligonucleotide Conjugate,” vol. 48, no. 8, pp. 565–578, 2024, doi: 10.20053/j.issn1001-5094.2024.08.002.
[3] S. J. Barker et al., “Targeting the transferrin receptor to transport antisense oligonucleotides across the mammalian blood-brain barrier,” Sci. Transl. Med., vol. 16, no. 760, 2024, doi: 10.1126/scitranslmed.adi2245.
[4] M. Kothari et al., “A Comprehensive Review of Monoclonal Antibodies in Modern Medicine: Tracing the Evolution of a Revolutionary Therapeutic Approach,” Cureus, vol. 16, no. 6, 2024, doi: 10.7759/cureus.61983.
[5] T. T. Hansel, H. Kropshofer, T. Singer, J. A. Mitchell, and A. J. T. George, “The safety and side effects of monoclonal antibodies,” Nat. Rev. Drug Discov., vol. 9, no. 4, pp. 325–338, 2010, doi: 10.1038/nrd3003.
[6] A. Toshima, Y. Shiraishi, D. Shinmi, Y. Kagawa, and J. Enokizono, “Comprehensive Analyses of the Intracellular and in Vivo Disposition of Fab– Small Interfering RNA Conjugate to Identify Key Issues to Improve Its in Vivo Activity,” Drug Metab. Dispos., vol. 51, no. 3, pp. 338–347, 2023, doi: 10.1124/dmd.122.001098.
[7] E. Holz, M. Darwish, D. B. Tesar, and W. Shatz-Binder, “A Review of Protein- and Peptide-Based Chemical Conjugates: Past, Present, and Future,” Pharmaceutics, vol. 15, no. 2, 2023, doi: 10.3390/pharmaceutics15020600.
[8] H. Lulu, R. Alexey, P. T. P, and N. Mehran, “CD29 TARGETTED OLIGONUCLEOTIDES AND USES THEREOF,” WO2025/006955A2, 2025
[9] M. Cochran et al., “Structure-Activity Relationship of Antibody-Oligonucleotide Conjugates: Evaluating Bioconjugation Strategies for Antibody-siRNA Conjugates for Drug Development,” J. Med. Chem., vol. 67, no. 17, pp. 14852–14867, 2024, doi: 10.1021/acs.jmedchem.4c00802.
[10] M. Egli and M. Manoharan, “Chemistry, structure and function of approved oligonucleotide therapeutics,” Nucleic Acids Res., vol. 51, no. 6, pp. 2529–2573, 2023, doi: 10.1093/nar/gkad067.
[11] C. Gareri, A. Polimeni, S. Giordano, L. Tamm, A. Curcio, and C. Indolfi, “Antisense Oligonucleotides and Small Interfering RNA for the Treatment of Dyslipidemias,” J. Clin. Med., vol. 11, p. 3884, 2022.
加入订阅
获取药物代谢与药代动力学最新专业内容和信息