中枢神经系统(CNS)疾病患病人数庞大,但CNS药物研发的临床实验成功率较低(约8%),不足其他药物如治疗心脑血管和感染疾病等药物成功率的一半[1],主要原因之一是使用临床前动物模型在预测人体CNS方面的准确性较低。在药代动力学方面,与人脑相比,啮齿类动物的脑组织构造、转运体类型和表达量都存在明显差异,使其难以成为转运体依赖型药物进行人体PK预测的理想模型动物;非人灵长类动物与人体脑组织有着极高的相似性,然而传统的PK研究方法需要在每个时间点牺牲动物采集脑组织,不符合动物福利伦理原则,阻碍其成为CNS药物研发的常规动物PK研究模型。
脑微透析(microdialysis)是一种在活体动物的脑组织中监测特定物质(如药物、神经递质和代谢产物等)浓度的技术。它通过在动物脑组织中植入微透析探针,可以实时监测脑内游离药物浓度的变化情况,为药物在脑内的暴露情况提供较为准确的量化数据,从而指导CNS药物的开发。关于微透析技术的更多介绍及其在啮齿动物上的应用请参考《微透析技术在药代动力学研究中的应用》。本文将在前文的基础上,进一步介绍猴脑微透析技术开发的背景、应用和必要性,以及药明康德DMPK关于猴脑微透析技术平台的建立和数据验证情况。
非人灵长类动物在CNS药物临床前药代动力学研究中展现出独特的模型优势,以下将从血脑屏障上转运蛋白的种属差异和一项CNS候选药物的回顾性分析两个方面展开阐述。
血脑屏障上转运蛋白的种属差异
基于特征肽段的液相色谱-串联质谱(LC-MS/MS)的定量方法对SD(Sprague-Dawley)大鼠、Wistar大鼠、食蟹猴和人脑毛细血管中血脑屏障功能蛋白的表达量进行比较。图1a和图1b对比了大鼠血脑屏障与人血脑屏障之间不同的转运蛋白表达量,SD大鼠和Wistar大鼠血脑屏障上的MDR1、MRP4、MCT1、TfR1和LAT-1蛋白表达水平比人高2倍以上,而BCRP、GLUT1、INSR、LRP1表达量差异小于2倍。如图2显示,食蟹猴血脑屏障上的MRP4、INSR、MDR1、BCRP、GLUT1和LRP1蛋白表达水平与人相近,而MCT1和GLUT3/14蛋白表达水平比人低2倍以上[2-5]。
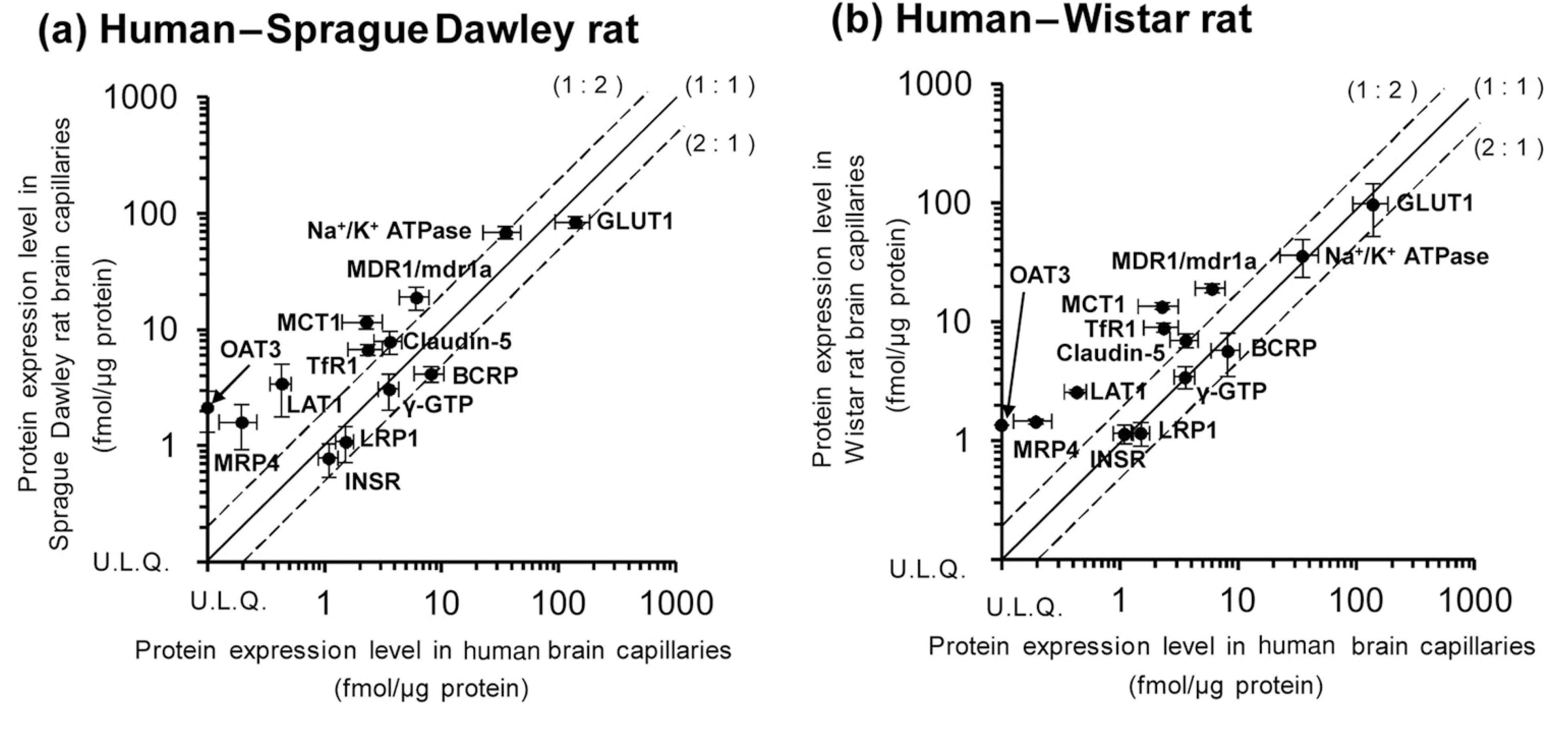
图1. 人和SD大鼠、Wistar大鼠脑毛细血管蛋白表达量比较[5]
血脑屏障上的ABC (ATP-binding cassette)转运蛋白,包括P-糖蛋白(P-gp)、乳腺癌耐药蛋白(BCRP)和多药耐药相关蛋白(MRP),能限制外来异物进入中枢神经系统,是阻止药物进入大脑的主要转运机制[6,7]。如表1所示,大鼠血脑屏障关键转运蛋白P-gp、BCRP、MRP4的表达量分别为19.1、4.71、1.53 fmol/g蛋白[4,5,8]。其中P-gp和MRP4两种关键转运蛋白在食蟹猴和人的血脑屏障上的表达量水平更加接近,而与大鼠差异较大。从血脑屏障上关键转运蛋白表达水平看,食蟹猴是预测转运体底物在人脑分布的较好模型,而使用大鼠预测可能导致结果偏离较大。关于更多的CNS药物筛选策略请参考《中枢神经系统药物药代动力学研究策略概述》。
表1. 大鼠、食蟹猴和人血脑屏障关键转运体蛋白P-gp、BCRP和MRP4表达量[4,5,8]
膜蛋白 | 血脑屏障膜蛋白表达量(fmol/g 蛋白) | ||
大鼠 | 食蟹猴 | 人 | |
P-gp | 19.1 | 4.71 | 6.06 |
BCRP | 4.15 | 14.2 | 8.14 |
MRP4 | 1.53 | 0.286 | 0.195 |
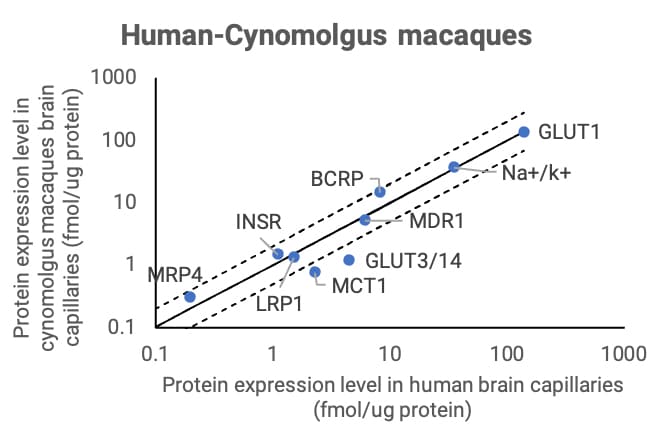
图2. 人和食蟹猴脑毛细血管蛋白表达量比较[3,4]
一项CNS候选药物的回顾性分析
在一项32种CNS候选药物的回顾性分析中,根据体外和体内研究的两个标准,将测试化合物按照如下两个标准分为三类,如图3所示。
标准一:体外试验中化合物是否为P-gp底物以及血脑屏障渗透性较低[9,10];
标准二:化合物在临床前物种(大鼠,小鼠或犬)中的体内分布是否达到血脑分布均衡[11,12]
第一类药物在体外实验中表现出良好的血脑屏障渗透性,并且不是P-gp底物,在体内临床前动物脑脊液(CSF)中的药物浓度、脑内游离药物浓度和血浆中游离药物浓度达到分布均衡(Kp,uu≈1,CSF中药物浓度或脑内游离药物浓度与血浆中游离药物浓度相当)。对于第一类化合物,检测人体游离血浆浓度可以用于推测人体脑内游离药物浓度,没有测量人体CSF中药物浓度的必要。临床研究中,无需采集人体CSF样本,这大大降低了人体CSF采样操作的安全风险。
第二类药物体外实验显示为非P-gp底物和良好的渗透性,但是临床前物种(大鼠、小鼠或狗)中血脑分布不均衡;或者是P-gp底物且渗透性差,但是临床前物种中(大鼠、小鼠或狗)达到血脑分布均衡,表现出体内外结果相互矛盾,因此很难预测人体中枢神经系统渗透性结果。但仍然有超过60%的该类药物表现出良好的人体中枢神经系统的渗透性。回顾性分析显示,并非所有的非P-gp底物都具有良好的血脑屏障渗透性,也有其他因素影响,包括其他关键转运蛋白(如BCRP、MRP)的参与、被动扩散的渗透性低等因素。
第三类药物是P-gp底物且渗透性差,临床前物种(大鼠、小鼠或狗)中未达到血脑分布均衡,临床前与临床结果均表明此类药物具有较差的渗透性,然而临床前和临床的渗透性结果仍然有较大差异,表明临床前数据不能用于预测这类药物在人脑中的暴露情况。转运蛋白表达差异和底物特异性的物种差异可能是使用临床前物种(大鼠、小鼠或狗)预测人脑渗透性不准确的原因。
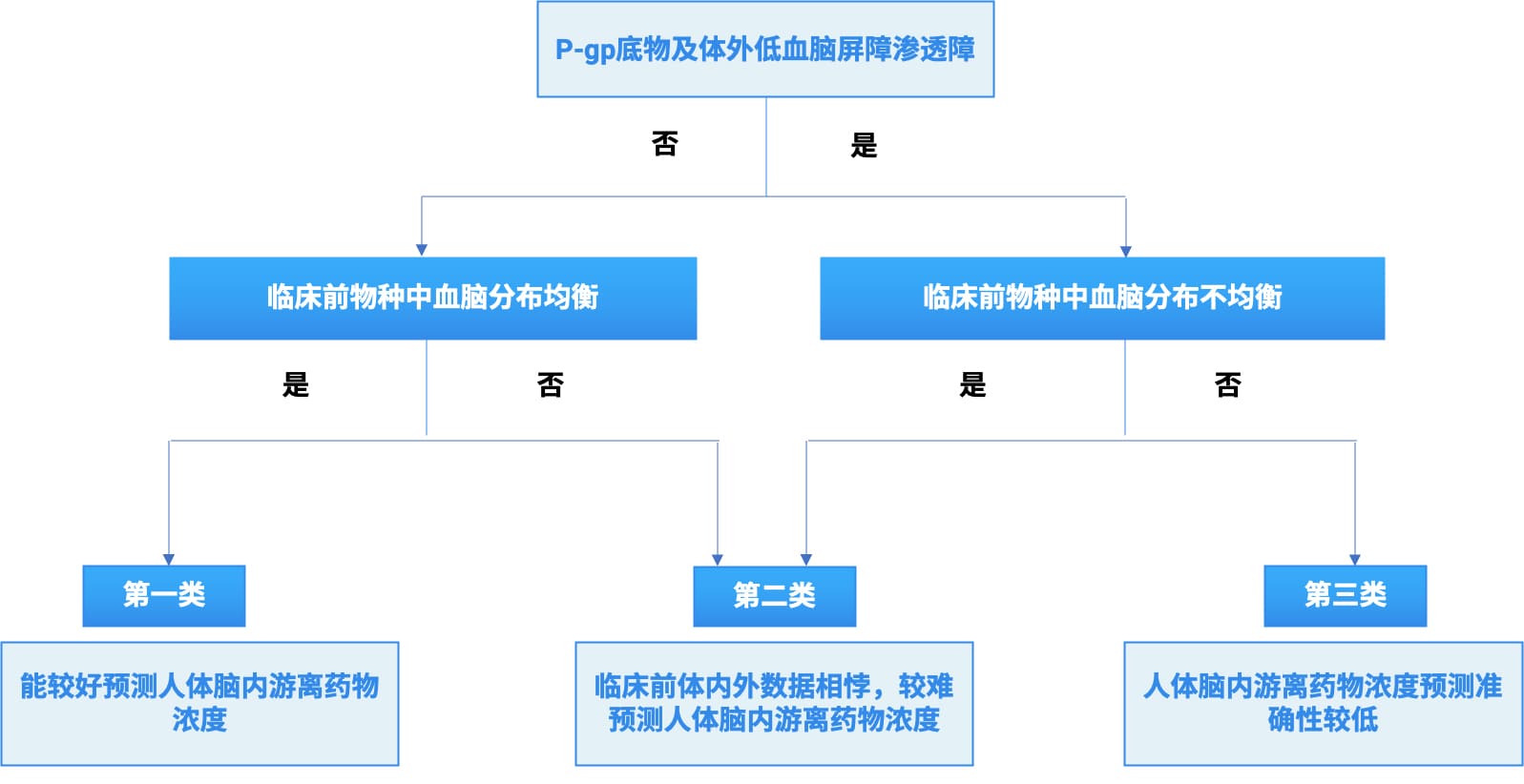
图3. CNS候选药物与人脑暴露数据的回顾性分析[12](临床前动物包括大鼠、小鼠和犬)
对于第二类和第三类化合物,预测其在人体脑内药物浓度具有一定挑战。而非人灵长类与人体相近的脑组织以及转运体表达量,为第二类和第三类化合物的临床预测提供了可能性。
猴脑微透析技术平台的建立和验证
非人灵长类动物(如猴子)的大脑结构与人类有更高的相似性,包括大脑皮层、边缘系统和其他重要区域,这使得猴子在脑组织分布方面的特征通常更接近于人类。

图4. 脑微透析示意图
猴脑微透析是在目标区域植入微透析探针。如图4所示,探针顶端的目标区域为脑纹状体。探针通常由一根细小的半透膜管组成,能够选择性地允许小于半透膜孔径的物质通过。在探针内注入人工脑脊液后,脑内的物质会通过半透膜进入探针内的溶液中,从而可以对其进行收集和分析。
使用猴脑进行微透析,与小动物(如小鼠或大鼠)探针和管道类似,故有相同的挑战,技术难度随膜孔径和亲脂性的增加而增加[13],而猴脑微透析存在更多难点和挑战,例如手术留置套管于颅顶后,容易被猴子破坏;而小动物无法破坏颅顶套管装置。药明康德DMPK通过对套管装置进行改进和升级,避免了猴子对颅顶套管装置的破坏,同时还可进行同一位点的多次微透析操作。
参考文献报道的猴脑微透析技术操作[14],结合已有的脑微透析技术储备及啮齿类动物微透析经验,选择非P-gp底物、通过被动扩散入脑的卡马西平作为验证药物,如果测得的脑内游离药物浓度和血浆中的游离药物浓度相当,可以证明猴脑微透析操作的可靠性。
对食蟹猴通过鼻灌胃分期给予15 mg/kg和7.5 mg/kg的卡马西平后,采集血液和脑纹状体的微透析液,来评估药物在血浆和猴脑组织中的分布情况。如图4所示,给药剂量分别为15 mg/kg和7.5 mg/kg时,脑细胞外液(ECF,extracellular fluid)的Cmax分别为982 ng/mL和531 ng/mL,具有明显的剂量浓度梯度关系。Cmax略高于文献值(同剂量下分别为693.4 ng/mL和321.6 ng/mL[14])。给药剂量分别为15 mg/kg和7.5 mg/kg时,ECF中药物暴露量和血浆中游离药物暴露量(AUC0-5h)比值分别为82.0%和77.5%,两个剂量下的比值结果一致,比文献报道值略低(113.9±7.5%[14]),与文献结果的差异可能与猴子的品系有关(文献为恒河猴数据,不排除因转运体蛋白差异等因素造成)。
综上,在食蟹猴脑微透析技术中,猴脑细胞外液Cmax、血脑游离药物暴露量AUC0-5h与文献报道基本一致,两组不同浓度的PK参数具有良好的剂量梯度关系。人体卡马西平脑细胞外液中的药物浓度和血浆中游离药物的浓度比值约为100%[15],与本实验测得的猴子血脑数据比较为接近。

图5. 食蟹猴体内血浆和脑透析液中卡马西平的药时曲线图
结 语
啮齿类动物脑微透析技术已经成为常规的CNS药物研发手段之一,但是在预测人脑药物分布方面,仅适用于非转运体底物且血脑分布均衡的化合物;猴脑微透析技术的开发为外排转运体底物的入脑评估提供了可靠的模型,可以在高度相关的动物模型中尽可能准确地预测药物在人脑中的药代动力学行为。药明康德DMPK不仅具备了猴脑微透析的能力,还建立了全面的神经系统药物研发平台,具备多种神经系统给药的能力和采样技术,如腰椎给药、侧脑室给药、小脑延髓池插管采集CSF等,能够全方位地助力CNS新药的研发。
作者:徐宾,汤里平,程起干,孙建平,刘守桃,金晶
编辑:富罗娜·克里木,钱卉娟
设计:倪德伟,张莹莹
药明康德DMPK依托中国(上海、苏州、南京和南通)和美国(新泽西)的研发中心,提供从早期筛选、临床前开发、到临床研究阶段的综合型药代动力学服务,助力您快速推进药物研发流程。拥有上千人的研发团队,服务超1600家全球客户,具有超过十五年的新药申报经验,已成功支持超过1700个新药临床研究申请(IND)。
点击此处与我们的专家进行联系。
参考
[1] Kola I, Landis J. Can the pharmaceutical industry reduce attrition rates? Nat Rev Drug Discov. 2004 Aug;3(8):711-5. doi: 10.1038/nrd1470. PMID: 15286737.
[2] Kamiie J, Ohtsuki S, Iwase R, Ohmine K, Katsukura Y, Yanai K, Sekine Y, Uchida Y, Ito S, Terasaki T. Quantitative atlas of membrane transporter proteins: development and application of a highly sensitive simultaneous LC/MS/MS method combined with novel in-silico peptide selection criteria. Pharm Res. 2008 Jun;25(6):1469-83. doi: 10.1007/s11095-008-9532-4. PMID: 18219561.
[3] Uchida Y, Ohtsuki S, Katsukura Y, Ikeda C, Suzuki T, Kamiie J, Terasaki T. Quantitative targeted absolute proteomics of human blood-brain barrier transporters and receptors. J Neurochem. 2011 Apr;117(2):333-45. doi: 10.1111/j.1471-4159.2011.07208.x. Epub 2011 Feb 25. PMID: 21291474.
[4] Ito K, Uchida Y, Ohtsuki S, Aizawa S, Kawakami H, Katsukura Y, Kamiie J, Terasaki T. Quantitative membrane protein expression at the blood-brain barrier of adult and younger cynomolgus monkeys. J Pharm Sci. 2011 Sep;100(9):3939-50. doi: 10.1002/jps.22487. Epub 2011 Jan 19. PMID: 21254069.
[5] Hoshi Y, Uchida Y, Tachikawa M, Inoue T, Ohtsuki S, Terasaki T. Quantitative atlas of blood-brain barrier transporters, receptors, and tight junction proteins in rats and common marmoset. J Pharm Sci. 2013 Sep;102(9):3343-55. doi: 10.1002/jps.23575. Epub 2013 May 6. PMID: 23650139.
[6] Ohtsuki S, Terasaki T. Contribution of carrier-mediated transport systems to the blood-brain barrier as a supporting and protecting interface for the brain; importance for CNS drug discovery and development. Pharm Res. 2007 Sep;24(9):1745-58. doi: 10.1007/s11095-007-9374-5. Epub 2007 Jul 10. PMID: 17619998.
[7] 谢振伟,臧彦楠,赵立波等.调控血脑屏障ABC转运体信号转导通路的研究现状[J].中国临床药理学杂志,2014(11):1057-1059.
[8] Syvänen S, Lindhe O, Palner M, Kornum BR, Rahman O, Långström B, Knudsen GM, Hammarlund-Udenaes M. Species differences in blood-brain barrier transport of three positron emission tomography radioligands with emphasis on P-glycoprotein transport. Drug Metab Dispos. 2009 Mar;37(3):635-43. doi: 10.1124/dmd.108.024745. Epub 2008 Dec 1. PMID: 19047468.
[9] Feng B, Mills JB, Davidson RE, Mireles RJ, Janiszewski JS, Troutman MD, de Morais SM. In vitro P-glycoprotein assays to predict the in vivo interactions of P-glycoprotein with drugs in the central nervous system. Drug Metab Dispos. 2008 Feb;36(2):268-75. doi: 10.1124/dmd.107.017434. Epub 2007 Oct 25. PMID: 17962372.
[10] Di L, Whitney-Pickett C, Umland JP, Zhang H, Zhang X, Gebhard DF, Lai Y, Federico JJ 3rd, Davidson RE, Smith R, Reyner EL, Lee C, Feng B, Rotter C, Varma MV, Kempshall S, Fenner K, El-Kattan AF, Liston TE, Troutman MD. Development of a new permeability assay using low-efflux MDCKII cells. J Pharm Sci. 2011 Nov;100(11):4974-85. doi: 10.1002/jps.22674. Epub 2011 Jul 15. PMID: 21766308.
[11] Rong, H.; Feng, B.; Di, L. Integrated Approaches to Blood Brain Barrier. In Encyclopedia of Drug Metabolism and Interactions; Lyubimov, A. V., Ed.; John Wiley & Sons: Hoboken, NJ, 2012.
[12] Di L, Rong H, Feng B. Demystifying brain penetration in central nervous system drug discovery. Miniperspective. J Med Chem. 2013 Jan 10;56(1):2-12. doi: 10.1021/jm301297f. Epub 2012 Nov 6. PMID: 23075026.
[13] Jadhav SB, Khaowroongrueng V, Derendorf H. Microdialysis of Large Molecules. J Pharm Sci. 2016 Nov;105(11):3233-3242. doi: 10.1016/j.xphs.2016.08.016. Epub 2016 Sep 23. PMID: 27671236.
[14] Thiollier T, Wu C, Porras G, Bezard E, Li Q, Zhang J, Contamin H. Microdialysis in awake macaque monkeys for central nervous system pharmacokinetics. Animal Model Exp Med. 2018 Dec 4;1(4):314-321. doi: 10.1002/ame2.12046. PMID: 30891581; PMCID: PMC6388052.
[15] Scheyer RD, During MJ, Spencer DD, Cramer JA, Mattson RH. Measurement of carbamazepine and carbamazepine epoxide in the human brain using in vivo microdialysis. Neurology. 1994 Aug;44(8):1469-72. doi: 10.1212/wnl.44.8.1469. PMID: 8058151.
加入订阅
获取药物代谢与药代动力学最新专业内容和信息














