近几十年来,除传统小分子药物外,新的治疗方法的开发取得了重大进展。蛋白降解靶向嵌合体即Proteolysis-Targeting Chimeras(在上下文中简称为“PROTAC”)就是一种新兴的分子治疗实体,PROTAC概念的提出起源于20年前,并在近几年如火如荼地发展(图1)。本文将针对PROTAC的作用机理、市场分析、DMPK研究难点以及研究策略进行一个概述,为PROTAC的临床前DMPK研究提供思路。

图1:PROTAC的发展历史
一、PROTAC的结构和作用机理
关于PROTAC的结构和作用机理,要从泛素-蛋白酶体通路讲起。2004年诺贝尔化学奖颁发给了Aaron Ciechanover、Avram Hershko和Irwin Rose,因为他们发现了泛素介导的蛋白质降解。
泛素(Ubiquitin)是一种由76个氨基酸组成的小蛋白,存在于所有已知的真核生物体中。泛素化过程主要由泛素激活酶E1,泛素结合酶E2和泛素连接酶E3介导。其中E1酶和E2酶参与的过程称为泛素的激活;E3酶与靶蛋白特异性结合,并催化泛素分子转移靶蛋白上,这一过程称为蛋白质的泛素化。经过这两个过程后,靶蛋白被泛素标记,最终被蛋白酶体(Proteasome)识别切割成小片段,实现靶蛋白的特异性降解(图2)。

图2:泛素介导的蛋白质降解过程[1]
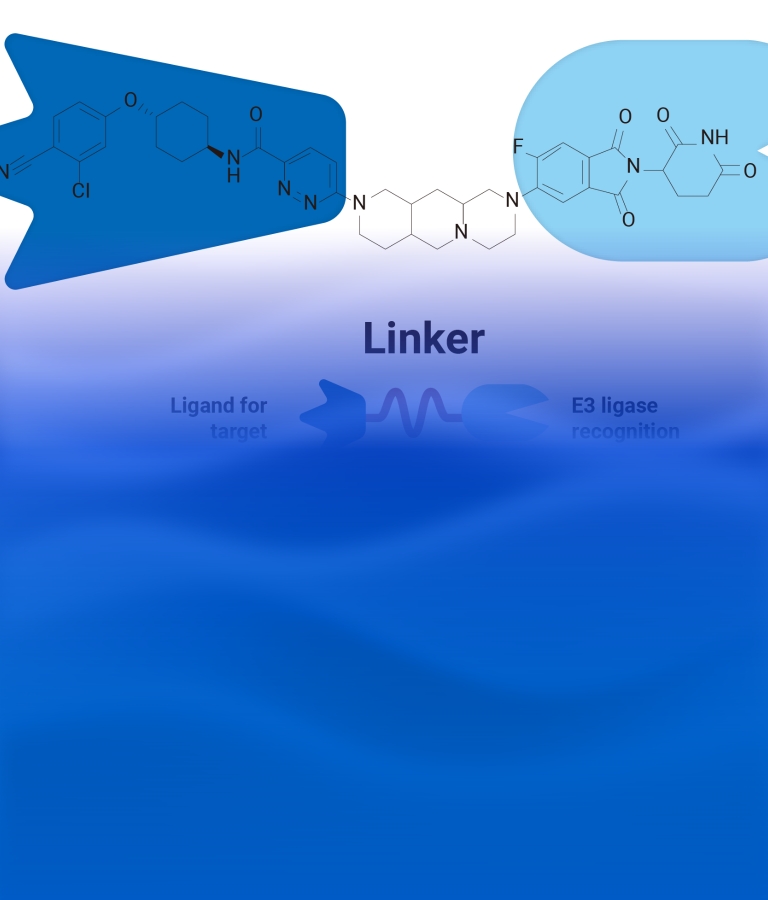
PROTAC,即蛋白水解靶向嵌合物,就利用了这一天然的蛋白降解机制。作为一种双功能分子,PROTAC由三个关键结构成分组成:一侧分子区域可结合E3连接酶,另一侧分子区域可结合靶蛋白,中间区域为接头分子(Linker)。

图3:PROTAC的结构示例
PROTAC依靠拉近E3连接酶和靶蛋白的距离,诱导E3连接酶为靶蛋白贴上泛素标签,继而促进靶蛋白的降解,靶蛋白降解后掉落下来的PROTAC分子可以继续地被循环利用(图3)。
我们知道,大多数小分子药物需要与酶或受体的活性位点结合才能发挥作用,这种作用机制被称为占据驱动模式,但是PROTAC可以通过任何一个角落、裂缝抓取蛋白从而降解蛋白,它不需要占据一个活跃的口袋工作,也不需要依赖靶标占有率来破坏靶标蛋白的功能,我们称之为事件驱动的药理学机制,也因此PROTAC为很多无活性位点的不可成药蛋白靶点的开发带来了希望;它还有望克服小分子的一些缺点比如耐药性,同时保留其直接作用于细胞内靶点的优势;且与抗体或寡核苷酸相比具有更高的口服生物利用度,还可以减少生产方面的挑战。

图4:PROTAC的作用机理[2]
二、PROTAC布局分析
PROTAC通过事件驱动的药理学提供了一个极具吸引力的治疗概念来控制目标蛋白的水平,尽管这是一种相对较新的模式,但它已经在药物发现的管线中取得了快速进展。
PROTAC研发进展——国际药企
随着Arvinas的两款候选分子ARV-110和ARV-471率先斩获积极的临床数据,这一领域在近两年迎来蓬勃发展,除此之外,该公司还有第三个PROTAC分子ARV-766即将进入临床阶段。另外一些专注于开发蛋白降解剂的国外公司,如Kymera Therapeutics、C4 Therapeutics和Nurix Therapeutics,他们各有一款分子处于临床Ⅰ期阶段。除此之外,一些其他的药企比如Bristol-Myers Squibb、Dialectic Therapeutics、Foghorn Therapeutics、Accutar Biotechnology、BeiGene也均有一个PROTAC分子处于临床Ⅰ期阶段。
|
公司 |
PROTAC |
适应症 |
靶点 |
研究阶段 |
|
Arvinas, Inc. |
ARV-110 |
转移性去势抵抗性前列腺癌(mCRPC) |
雄激素受体(AR) |
临床Ⅱ期 |
|
ARV-471 |
乳腺癌(ER+/HER2-Breast Cancer) |
雌激素受体(ER) |
临床Ⅱ期 |
|
|
ARV-766 |
转移性去势抵抗性前列腺癌(mCRPC) |
AR |
临床Ⅰ期 |
|
|
AR-V7 |
转移性去势抵抗性前列腺癌(mCRPC) |
AR-FL & AR-V7 |
临床前 |
|
|
Nurix Therapeutics, Inc. |
NX-2127 |
B细胞恶性肿瘤 |
BTK + IMiD Activity |
临床Ⅰ期 |
|
NX-5948 |
B细胞恶性肿瘤及自身免疫类疾病 |
BTK |
临床Ⅰ期 |
|
|
Kymera Therapeutics, Inc. |
KT-474 |
过敏性皮炎、化脓性汗腺炎、类风湿性关节炎 |
白细胞介素-1受体相关激酶4(IRAK4) |
临床Ⅰ期 |
|
KT-333 |
肿瘤 |
STAT3 |
临床Ⅰ期 |
|
|
KT-413 |
MYD88基因突变的B细胞淋巴瘤 |
IRAK4 |
临床Ⅰ期 |
|
|
C4 Therapeutics, Inc. |
CFT7455 |
复发/难治性非霍奇金淋巴瘤或多发性骨髓瘤 |
IKZF1/3 |
临床Ⅰ/Ⅱ期 |
|
CFT8919 |
产生耐药性的EGFR突变的非小细胞肺癌(NSCLC) |
EGFR L858R |
IND申报 |
|
|
CFT8634 |
滑膜肉瘤和smarcb1缺失实体瘤 |
BRD9 |
临床Ⅰ/Ⅱ期 |
|
|
Bristol-Myers Squibb |
AR-LDD |
前列腺癌 |
AR |
临床Ⅰ期 |
|
Dialectic Therapeutics, Inc. |
DT-2216 |
肿瘤 |
BCL-XL |
临床Ⅰ期 |
|
Foghorn Therapeutics, Inc. |
FHD-609 |
滑膜肉瘤 |
BRD9 |
临床Ⅰ期 |
|
Accutar Biotechnology Inc. |
AC0682 |
乳腺癌 |
ER |
临床Ⅰ期 |
|
AC0176 |
前列腺癌 |
AR |
临床Ⅰ期 |
|
|
AC0676 |
自身免疫 |
BTK WT & C481S |
IND申报 |
表1. 部分国际药企的PROTAC研发进展
注:信息来源于上述公司官网,信息收集截止日期2022年12月16日。
PROTAC研发进展——中国药企
在中国,也有不少企业正在开发PROTAC分子,比如凌科药业、开拓药业、海思科、美志医药、睿跃生物、海创药业和万春医药子公司Seed Therapeutics等均已在PROTAC领域布局。其中,凌科药业、开拓药业、海思科均有一款PROTAC分子进入临床Ⅰ期阶段。
|
公司 |
PROTAC |
适应症 |
靶点 |
研究阶段 |
|
凌科药业(杭州)有限公司 |
LNK01002 |
血液肿瘤 |
— |
临床Ⅰ期 |
|
苏州开拓药业股份有限公司 |
GT20029 |
雄激素性脱发、痤疮 |
AR |
临床Ⅰ期 |
|
海思科医药集团股份有限公司 |
HSK29116 |
B细胞恶性肿瘤 |
BTK |
临床Ⅰ期 |
|
上海美志医药科技有限公司 |
MZ-001 |
B细胞恶性肿瘤和自身免疫疾病 |
BTK |
IND申报 |
|
百济神州有限公司 |
BGB-16673 |
B细胞恶性肿瘤 |
BTK |
临床Ⅰ期 |
|
上海睿跃生物科技有限公司 |
CG416 |
— |
神经营养因子受体酪氨酸激酶(TRK) |
临床前 |
|
CG428 |
— |
TRK |
临床前 |
|
|
CG001419 |
— |
TRK |
临床Ⅰ/Ⅱ期 |
|
|
海创药业股份有限公司 |
HP518 |
标准治疗失败的mCRPC |
AR |
临床Ⅰ期 |
|
HC-X029 |
标准治疗失败的mCRPC的末线治疗 |
AR-sv |
临床前 |
|
|
HC-X035 |
KRAS突变癌症 |
含有两个SH2(Src homology-2)域的蛋白酪氨酸磷酸酶(SHP2) |
临床前 |
表2. 部分中国药企的PROTAC研发进展
注:信息来源于上述公司官网,信息收集截止日期2022年12月16日。
PROTAC公司与药企巨头合作情况
随着靶向蛋白降解疗法受到越来越多的关注,多家专注于PROTAC开发的新锐公司或具有PROTAC研发管线的公司也获得了与药企巨头合作的机会,例如Arvinas、Kymera Therapeutics、C4 Therapeutics、Nurix Therapeutics、Vividion、万春医药子公司Seed Therapeutics等公司。
|
PROTAC公司 |
时间 |
合作药企 |
合作内容 |
投资情况 |
|
Arvinas, Inc. |
2021年7月 |
辉瑞 |
Arvinas和辉瑞宣布全球合作开发PROTAC®蛋白降解剂ARV-471并商业化 |
6.5 亿美元预付款、 |
|
2019年6月 |
拜耳 |
拜耳和 Arvinas 推出靶向蛋白质降解合资企业 Oerth Bio开发创新农产品来提高作物产量 |
1.1亿美元投资 |
|
|
2018年1月 |
辉瑞 |
Arvinas 宣布与辉瑞公司就蛋白质降解候选药物的发现和开发达成研究合作和许可协议 |
8.3 亿美元预付款、 |
|
|
2017年11月 |
罗氏(基因泰克) |
Arvinas 扩大与基因泰克的战略许可协议 |
增加至超过 6.5 亿美元的开发和商业化里程碑付款 |
|
|
2015年10月 |
罗氏(基因泰克) |
Arvinas 与基因泰克签署战略许可协议 |
超过 3 亿美元开发和商业化里程碑付款 |
|
|
2015年4月 |
默克 |
Arvinas与默克公司战略研发合作,研究新型蛋白质降解技术 |
4.34 亿美元里程碑付款 |
|
|
Kymera Therapeutics, Inc. |
2020年7月 |
赛诺菲 |
向患者推进新型蛋白质降解剂疗法 |
1.5 亿美元预付款 |
|
2019年3月 |
Vertex |
发现和开发针对严重疾病的靶向蛋白质降解药物 |
7000 万美元的预付款、股权投资、以及合作中最多六个项目的潜在额外里程碑和特许权使用费 |
|
|
2018年4月 |
葛兰素史克 |
Kymera Therapeutics 宣布与葛兰素史克开展研发合作以推进新的治疗方式 |
— |
|
|
C4 Therapeutics, Inc. |
2019年1月 |
百健 |
使用 C4T 的蛋白质降解平台,用于发现和开发针对神经系统疾病(如阿尔茨海默病和帕金森病)的潜在新疗法 |
4.15 亿美元的预付款、潜在的未来里程碑付款以及潜在的未来特许权使用费 |
|
2019年1月 |
罗氏 |
专注于基于 C4T 靶向蛋白质降解技术的新癌症治疗方法 |
9 亿美元的预付款、潜在的未来里程碑付款 |
|
|
Nurix Therapeutics, Inc. |
2021年1月 |
赛诺菲 |
扩大协议 |
增加2200 万美元的预付款 |
|
2020年1月 |
赛诺菲 |
发现、开发和商业化一系列创新的靶向蛋白质降解药物,用于多个治疗领域的具有挑战性的疾病 |
5500 万美元的预付款, |
|
|
2019年6月 |
吉利德 |
发现、开发和商业化一系列创新的靶向蛋白质降解药物,吉利德将有权选择许可针对最多五个靶标的候选药物 |
4500 万美元的预付款, |
|
|
Vividion Therapeutics, Inc. |
2020年3月 |
罗氏 |
PROTAC早期药物发现及临床前研究 |
1.35亿美元及高达数十亿的潜在里程碑付款 |
|
2021年8月 |
拜耳 |
8月5日,拜耳集团宣布收购Vividion,获得 Vividion 专有发现平台的全部权利 |
拜耳将支付15亿美元的预付款项以及基于目标成功达成、最高可达5亿美元的里程碑付款 |
|
|
Seed Therapeutics, Inc. |
2020年11月 |
礼来 |
共同研究开发一类通过靶向蛋白降解(TPD)而发挥治疗作用的新化学实体 |
1000万美元首付款、7.9亿美元的里程碑付款以及1000万美元的股权投资 |
表3. PROTAC公司与药企巨头合作情况
注:信息来源于上述公司官网。
三、PROTAC药物研发的DMPK难点与重要性
尽管PROTAC技术因为其独特的作用机制受到青睐,但PROTAC分子的开发也依然面临着多方挑战(图5)。

图5:PROTAC的研发难点与重要性
口服给药是大多数疾病治疗的理想给药方式,但是由于PROTAC独特的结构导致分子量较大,溶解性较差,药物性质很难满足经典的Lipinski类药五原则。并且其体内外渗透性表现不佳,口服生物利用度通常偏低,吸收较差。
对于传统的小分子抑制剂,通常暴露量越高活性越好。但PROTAC的多项研究表明在适当的或低浓度下会形成正常的三元复合物,而在高浓度时会观察到钩子效应(图6),即高浓度时会竞争性地形成靶蛋白-PROTAC或E3连接酶-PROTAC二元复合物,导致药效降低或出现毒性反应。这就需要对PROTAC的PKPD性质足够了解,及时调整剂量。

图6:钩子效应示意图
此类分子在各种属中均呈现较高的血浆蛋白结合,利用常规的血浆蛋白结合检测方法未必能准确测定其血浆蛋白结合率;高血浆蛋白结合也减缓了它们的代谢,不易被清除,有些化合物则会在血浆中进行代谢。
由于其结构的特殊性,代谢产物生成会导致不可预知的蛋白降解,导致药效丧失,甚至产生毒性反应,因此体内代谢产物的监测为其临床前筛选至关重要的一环,尤其需要关注linker断裂型代谢产物。
目前没有专门针对PROTAC药物的指导原则,在实际研究中,一般会根据具体情况参照小分子药物的指导原则。药明康德DMPK团队,基于过往该类药物开发的经验,依托部门完善的体外体内药代动力学测试平台,结合PROTAC技术原理与特点,建立起一套关于PROTAC药物DMPK筛选和评价的通用体系,在临床前制剂筛选、DMPK实验设计、体外实验方法的选择、生物样品分析速度、体内外代谢产物鉴定能力、筛选策略及跨部门合作等各个方面都有着突出优势,有效缩短PROTAC的开发周期(图7)。

图7:药明康德DMPK在PROTAC研究中的优势
四、PROTAC药物DMPK研究的策略和流程
PROTAC药物的临床前优化主要通过理化性质和DMPK性质的级联优化来进行(图8)。

图8:PROTAC药物DMPK研究的策略和流程[3]
01 首先需要进行PROTAC分子的体内外性质表征,以此进行初步的筛选,包含理化性质、渗透性、蛋白结合以及药物相互作用。
02 在优化阶段主要专注于改善PROTAC的代谢清除和溶解度,结合血管外给药的PK性质来建立合适的模型以便更好地了解PROTAC的吸收与代谢等DMPK性质。PROTAC的渗透性虽然对吸收很重要,但是基于其结构和分子量大的特点,不太可能得到显著改善,因此对于口服的PROTAC而言,在优化阶段会更加关注溶解度。
03 在PCC阶段,强效且口服生物利用度较优的PROTAC分子可以用于进一步的PK/PD研究,从而得到更深入的暴露量-反应性关系(Exposure-response relationship)。
结语
虽然目前PROTAC并没有上市药物,却吸引着越来越多的生物医药创新者和创业者在这个全新的赛道上竞相角逐。在20多年的发展中,PROTAC以其独特的作用模式将小分子重新定义,它突破了一直以来大家认可的成药规则,却在不断的探索与前进中为新药开发打开了新篇章。药明康德DMPK有着多年的PROTAC研究经验、专业的PROTAC研究团队、完善的PROTAC研究平台,我们期待越来越多的PROTAC分子被设计和开发,在更多的疾病领域解锁新的机遇,也为更多的患者带去希望。
药明康德DMPK依托在中国(上海、苏州、南京和南通)和美国(新泽西)的研发中心,提供从早期筛选、临床前开发、到临床研究阶段的综合型药代动力学服务,助力您快速推进药物研发流程。拥有上千人的研发团队,服务超1500家全球客户,具有超过十五年的新药申报经验,已成功支持超过1200个新药临床研究申请(IND)。
点击此处可与我们的专家进行联系。
作者:李成园,王宇,金晶
编辑:方健,钱卉娟
设计:倪德伟
参考
[1] Balint Földesi, Paul Domanski. Recycling the Cell: Autophagy and the Ubiquitin-Proteasome Processes.biomol-blog, 2019.
[2] Churcher I .Protac-induced Protein Degradation in Drug Discovery: Breaking the Rules - or Just Making New Ones?. Journal of Medicinal Chemistry, 2018, 61(2):444-452.
[3] Cantrill C ,Chaturvedi P , Rynn C , et al. Fundamental aspects of DMPK optimization of targeted protein degraders. Drug Discovery Today, 2020, 25(6):969-982
加入订阅
获取药物代谢与药代动力学最新专业内容和信息